题目内容
6.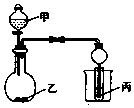 用如图装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中对应选项正确的是 ( )
用如图装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中对应选项正确的是 ( ) | 甲 | 乙 | 丙 | 试管中的现象 | |
| A | 浓硫酸 | 亚硫酸钠 | 石蕊试液 | 先变红后褪色 |
| B | 浓硝酸 | 铜 | KI-淀粉溶液 | 溶液变蓝色 |
| C | 醋酸 | 粉末状贝壳 | BaCl2溶液 | 变浑浊 |
| D | 浓氨水 | 生石灰 | FeCl2溶液 | 最后生成白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.浓硫酸与亚硫酸钠反应生成二氧化硫,二氧化硫为酸性氧化物;
B.浓硝酸与Cu反应生成二氧化氮,二氧化氮与水反应生成硝酸,硝酸可氧化KI;
C.醋酸与粉末状贝壳反应生成二氧化碳,但二氧化碳与氯化钡不反应;
D.混合生成氨气,氨气与FeCl2溶液反应生成的氢氧化亚铁易被氧化.
解答 解:A.浓硫酸与亚硫酸钠反应生成二氧化硫,二氧化硫为酸性氧化物,遇石蕊变红,现象不合理,故A错误;
B.浓硝酸与Cu反应生成二氧化氮,二氧化氮与水反应生成硝酸,硝酸可氧化KI,生成碘遇淀粉变蓝,则溶液变蓝色,故B正确;
C.醋酸与粉末状贝壳反应生成二氧化碳,但二氧化碳与氯化钡不反应,丙中无现象,故C错误;
D.混合生成氨气,氨气与FeCl2溶液反应生成的氢氧化亚铁易被氧化,丙中白色沉淀迅速变为灰绿色,最后为红褐色,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的性质及反应现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列说法中,正确的是(设阿伏加德罗常数的数值为6.02×1023)( )
| A. | MgCl2 的摩尔质量为95 g | |
| B. | 常温常压下,1 mol CO2的质量是44 g | |
| C. | 标准状况下,1 mol H2O所占的体积约为22.4 L | |
| D. | 100 mL 1mol/L的稀硫酸中含有H+ 的数目约为6.02×1022 |
17.用下列试剂和试管中的物质不能完成相应实验目的是( )
| 实验目的 | 试剂 | 试管中的物质 |  | |
| A | 苯环对甲基的影响 | 酸性KMnO4溶液 | ①苯②甲苯 | |
| B | 比较Br-、Fe2+和I-的还原性 | 氯水 | ①FeBr2溶液②FeI2溶液 | |
| C | 苯分子中没有碳碳双键 | Br2的CCl4溶液 | ①苯②己烯 | |
| D | 探究接触面积对反应速率的影响 | VmL、cmol/L的盐酸 | ①ag大理石块②ag大理石粉 |
| A. | A | B. | B | C. | C | D. | D |
14.某海域海水一些化学成分如表:
已知:25℃时,Ksp(CaCO3)=2.8×10-9、Ksp(MgCO3)=6.8×10-6,Ksp=1.8×10-11.
某化学小组同学欲用该海水制备MgCl2,并提取Zn.设计流程如图:
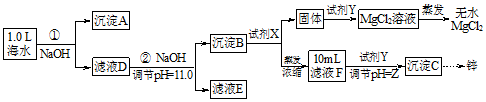
(1)写出生成沉淀A的化学方程式HCO3-+OH-+Ca2+=CaCO3↓+H2O.
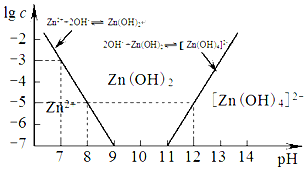
(2)如图为溶液pH与对应的Zn2+、2-物质的量浓度的对数坐标图,结合图中数据,由滤液F到沉淀C过程(一般认为离子浓度低于10-5 mol/L就是沉淀完全),则调节的pH的范围为8<pH<12.
(3)把MgCl2溶液蒸发得到无水MgCl2时,蒸发操作应该在在HCl气氛中环境中进行.
(4)试剂X为NaOH(写化学式).
| 海水成分 | Na+ | Ca2+ | Mg2+ | HCO3- | Zn2+ |
| 含量/mol•L-1 | 0.4 | 0.002 | 0.045 | 0.002 | 10-7 |
某化学小组同学欲用该海水制备MgCl2,并提取Zn.设计流程如图:

(1)写出生成沉淀A的化学方程式HCO3-+OH-+Ca2+=CaCO3↓+H2O.
(2)如图为溶液pH与对应的Zn2+、2-物质的量浓度的对数坐标图,结合图中数据,由滤液F到沉淀C过程(一般认为离子浓度低于10-5 mol/L就是沉淀完全),则调节的pH的范围为8<pH<12.

(3)把MgCl2溶液蒸发得到无水MgCl2时,蒸发操作应该在在HCl气氛中环境中进行.
(4)试剂X为NaOH(写化学式).
1.配制500mL 1mol•L-1的NaCl溶液时,下列实验操作会使配得的溶液浓度偏大的是( )
| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | 称量时左码右物 | |
| C. | 定容后把容量瓶倒转摇匀,发现液面低于刻度,再滴加几滴水至刻度线 | |
| D. | 在容量瓶中进行定容时俯视刻度线 |
11.下列有水参加反应中,属于氧化还原但水即不是氧化剂也不是还原剂的是( )
| A. | CaH2+2H2O═Ca(OH)2+2H2↑ | B. | 2F2+2H2O═4HF+O2 | ||
| C. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | D. | 2Na2O2+H2O═4NaOH+O2↑ |
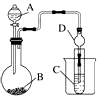 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.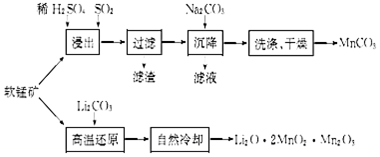
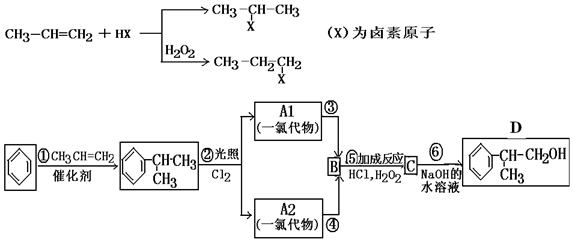
 ;
;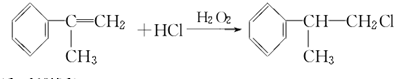 ;
;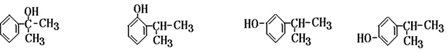 .
.