题目内容
下列各组离子,在强酸性溶液中可以大量共存的是( )
| A、Fe3+、NH4+、NO3-、Cl- |
| B、K+、Na+、SO42-、AlO2- |
| C、Cu2+、Fe2+、OH-、NO3- |
| D、NH4+、K+、HCO3-、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:酸性溶液中含大量的H+,根据离子之间不能结合生成水、气体、沉淀等,不能发生氧化还原反应,则可大量共存,以此来解答.
解答:
解:A.酸性条件下,离子之间不发生任何反应,大量共存,故A正确;
B.酸性条件下AlO2-不能大量共存,故B错误;
C.酸性条件下OH-不能大量共存,且Fe2+与NO3-发生氧化还原反应,故C错误;
D.酸性条件下HCO3-不能大量共存,故D错误.
故选A.
B.酸性条件下AlO2-不能大量共存,故B错误;
C.酸性条件下OH-不能大量共存,且Fe2+与NO3-发生氧化还原反应,故C错误;
D.酸性条件下HCO3-不能大量共存,故D错误.
故选A.
点评:本题考查离子的共存,为高考常见题型,侧重信息的抽取和氧化还原反应的考查,注重学生思维严密性的训练,有利于提高学生分析问题解决问题的能力,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列分子中属于非极性分子的是( )
| A、H2O |
| B、CH4 |
| C、NH3 |
| D、HCl |
在一定条件下,将1mol CO和1mol水蒸气混合后发生如下变化:CO(g)+H2O(g)?CO2(g)+H2(g)若反应达平衡时测得CO转化率为25%,则平衡混合气体的密度为相同条件下H2密度的( )
| A、5.75倍 | B、11.5倍 |
| C、30.67倍 | D、46倍 |
一定条件下体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),60s时达到平衡,生成0.3mol Z.下列说法正确的是( )
| A、反应进行30s时,正反应速率等于逆反应速率 |
| B、反应进行80s时,逆反应速率大于正反应速率 |
| C、这段时间内以X的浓度变化表示的反应速率为0.001mol/(L?s) |
| D、反应进行80s时,X物质的量浓度为0.4mol/L |
铁和稀硫酸在敞口容器中进行反应:Fe+H2SO4=FeSO4+H2↑,下列叙述不正确的是( )
A、该反应的反应过程与能量关系可以用图表示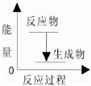 |
| B、若将该反应设计成原电池,当正极产生22.4L气体时,有56g铁溶解 |
| C、若将该反应设计成原电池,溶液中SO42-向Fe电极移动 |
| D、若将该反应设计成原电池,负极发生的反应是:Fe-2e=Fe2+ |
下列与有机物结构、性质相关的叙述错误的是( )
| A、苯酚分子中含有羟基,不与NaHCO3溶液反应生成CO2 |
| B、溴乙烷含溴原子,在氢氧化钠的乙醇溶液共热下发生取代反应 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| D、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
 某烃的结构简式如图,分子中含有四面体结构的碳原子(即饱和碳原子)数为x,在同一直线上的碳原子数为y,一定在同一平面上的碳原子数为z,则 x、y、z分别为( )
某烃的结构简式如图,分子中含有四面体结构的碳原子(即饱和碳原子)数为x,在同一直线上的碳原子数为y,一定在同一平面上的碳原子数为z,则 x、y、z分别为( )| A、4,3,5 |
| B、5,5,4 |
| C、5,3,6 |
| D、4,6,4 |
下列化合物中,含有共价键的是( )
| A、NaCl |
| B、He |
| C、NaOH |
| D、CaCl2 |