题目内容
5.下列排列有错误的是( )| A. | 粒子半径:F->Na+>Mg2+>Al3+ | B. | 稳定性:HI>HBr>HCl>HF | ||
| C. | 酸性:H4SiO4<H3PO4<H2SO4<HClO4 | D. | 碱性:Al(OH)3<Mg(OH)2<Ca(OH)2<KOH |
分析 A、电子层结构相同核电荷数越大,离子半径越小,电子层越多离子半径越大;
B、元素非金属性越强,对应的氢化物越稳定越强;
C、元素的非金属性越强,其最高价氧化物的水合物的酸性越强;
D、元素金属性越强,其最高价氧化物的水化物碱性越强.
解答 解:A、Na+、Mg2+、Al3+、F-离子核外电子排布相同,核电核数F<Na<Mg<Al,则半径F2->Na+>Mg2+>Al3+,故A正确;
B、元素非金属性:I<Br<Cl<F,所以对应的氢化物越稳定:HI<HBr<HCl<HF,故B错误;
C、元素的非金属性:Si<P<S<Cl,所以酸性:H4SiO4<H3PO4<H2SO4<HClO4,故C正确;
D、元素金属性Al<Mg<Ca<K,所以碱性:Al(OH)3<Mg(OH)2<Ca(OH)2<KOH,故D正确;
故选B.
点评 本题考查元素周期表和元素周期律的应用,为高频考点,把握元素的位置、性质的变化规律为解答的关键,侧重金属性、非金属性比较的考查,题目难度不大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
15. 如图所示,电流表G的指针发生偏转,同时A极质量增加,B极质量减少,C为电解质溶液.则A、B、C分别为( )
如图所示,电流表G的指针发生偏转,同时A极质量增加,B极质量减少,C为电解质溶液.则A、B、C分别为( )
 如图所示,电流表G的指针发生偏转,同时A极质量增加,B极质量减少,C为电解质溶液.则A、B、C分别为( )
如图所示,电流表G的指针发生偏转,同时A极质量增加,B极质量减少,C为电解质溶液.则A、B、C分别为( )| A. | A是Zn,B是Cu,C是稀硫酸 | B. | A是Cu,B是Zn,C是稀硫酸 | ||
| C. | A是Fe,B是Ag,C是AgNO3稀溶液 | D. | A是Ag,B是Fe,C是AgNO3稀溶液 |
16.反应3Fe(s)+4H2O(g)$\stackrel{高温}{?}$Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变会使化学反应速率加快的是( )
| A. | 增加Fe的量 | |
| B. | 将容器的容积缩小一半 | |
| C. | 保持容积不变,充入N2使体系压强增大 | |
| D. | 压强不变,充入N2使容器容积增大 |
20.下列高分子化合物所对应的结构单元正确的是( )
| A. | 聚氯乙烯  | B. | 聚苯乙烯  | ||
| C. | 聚异戊二烯 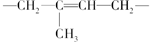 | D. | 聚丙烯-CH2-CH2-CH2- |
10.下列叙述正确的是( )
| A. | pH=2的硫酸溶液中c(H+):c(SO42-)等于2:1,稀释100倍后二者的比值几乎不变 | |
| B. | 由水电离的c(H+)=10-12mol/L的溶液中K+、Ba2+、Cl-、Br-、HCO3-一定能大量共存 | |
| C. | 1.0×10-3mol/L盐酸的pH=3,则1.0×10-8mol/L盐酸的pH=8 | |
| D. | 某温度下水的离子积为1×10-12,若使pH=1的H2SO4溶液与pH=12的NaOH溶液混合后溶液呈中性,则两者的体积比为1:10 |
14.下列是一些化学键的键能.
根据键能数据估算下列反应CH4 (g)+4F2 (g)═CF4+4HF(g)的反应热△H为( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | -1940 kJ•mol-1 | B. | 1940 kJ•mol-1 | C. | -485 kJ•mol-1 | D. | 485 kJ•mol-1 |


 .
. B、
B、 C、
C、 D、
D、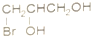

 ,其化学键的类型为离子键、共价键.
,其化学键的类型为离子键、共价键.