题目内容
饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为如下:
10Al+2NaNO3+4NaOH→10NaAlO2+3N2↑+2H2O.请回答下列问题:
①上述反应中, 元素的化合价升高,则该元素的原子 (填“得到”或“失去”)电子.
②用“单线桥法”表示上述反应中电子转移的方向和数目 :
10Al+2NaNO3+4NaOH→10NaAlO2+3N2↑+2H2O.请回答下列问题:
①上述反应中,
②用“单线桥法”表示上述反应中电子转移的方向和数目
考点:氧化还原反应
专题:氧化还原反应专题
分析:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,Al元素化合价升高,被氧化,N元素化合价降低,被还原,结合化合价的变化判断电子的得失以及电子转移的方向和数目.
解答:
解:(1)Al元素的化合价升高,失去电子,故答案为:Al;失去;
(2)10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,Al元素化合价升高,被氧化,在反应中失去电子,铝失去电子数为10×3,NaNO3得到电子数为6×5,则用“单线桥法”标明反应中电子转移的方向和数目为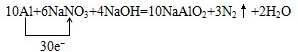 ,
,
故答案为: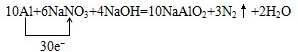 .
.
(2)10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,Al元素化合价升高,被氧化,在反应中失去电子,铝失去电子数为10×3,NaNO3得到电子数为6×5,则用“单线桥法”标明反应中电子转移的方向和数目为
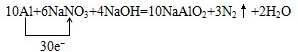 ,
,故答案为:
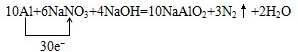 .
.
点评:本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
我国古代湿法炼铜的反应原理是( )
A、CuO+H2
| ||||
B、CuO+CO
| ||||
| C、CuSO4+Fe═Cu+FeSO4 | ||||
D、2CuO+C
|
Cl2和SO2都具有漂白作用,若将等物质的量的这两种气体混合通入品红中,能观察到的现象是( )
| A、溶液很快褪色 |
| B、溶液不褪色 |
| C、出现沉淀 |
| D、溶液变成黄绿色 |
 D.
D.