题目内容
(1)下列物质所含分子数由多到少的排列顺序是 ,
A.标准状况下33.6L H2 B.所含电子的物质的量为4mol的H2
C.20℃45g H2O D.常温下,16g O2与14g N2的混合气体
E.含原子总数约为1.204×1024的NH3
(2)用量筒量取一定体积的液体时,若采用俯视的方法量取20ml液体,则实际量取的液体的体积比20ml ,若量筒中实际有20ml液体,而你读数时采用了俯视的方法,则读得的数据比20ml .
(3)在BaCl2溶液中加入一定量的稀硫酸,恰好完全反应,产生的沉淀质量与原稀硫酸溶液的质量相同,则原稀硫酸溶液中溶质的质量分数是 .(结果保留4位有效数字)
A.标准状况下33.6L H2 B.所含电子的物质的量为4mol的H2
C.20℃45g H2O D.常温下,16g O2与14g N2的混合气体
E.含原子总数约为1.204×1024的NH3
(2)用量筒量取一定体积的液体时,若采用俯视的方法量取20ml液体,则实际量取的液体的体积比20ml
(3)在BaCl2溶液中加入一定量的稀硫酸,恰好完全反应,产生的沉淀质量与原稀硫酸溶液的质量相同,则原稀硫酸溶液中溶质的质量分数是
考点:物质的量的相关计算,溶液中溶质的质量分数及相关计算
专题:计算题
分析:(1)计算出各物质的物质的量,再比较分子数多少;
(2)量筒的刻度由上到下逐渐减小以及俯视时液面低于刻度线;
(3)根据硫酸与氯化钡反应的化学方程式,可以求出硫酸与硫酸钡之间的质量关系,由于产生沉淀的质量和原硫酸溶液的质量相等,也是硫酸与硫酸溶液的之间质量关系,根据这个质量关系即可求出则原硫酸溶液中溶质的质量分数.
(2)量筒的刻度由上到下逐渐减小以及俯视时液面低于刻度线;
(3)根据硫酸与氯化钡反应的化学方程式,可以求出硫酸与硫酸钡之间的质量关系,由于产生沉淀的质量和原硫酸溶液的质量相等,也是硫酸与硫酸溶液的之间质量关系,根据这个质量关系即可求出则原硫酸溶液中溶质的质量分数.
解答:
解:(1)A.标准状况下33.6L H2 物质的量为1.5mol;
B.所含电子的物质的量为4mol的H2物质的量为2mol;
C.20℃45g H2O物质的量为2.5mol;
D.常温下,16g O2与14g N2的混合气体,物质的量为1mol;
E.含原子总数约为1.204×1024的NH3,物质的量为0.25mol;
则物质所含分子数由多到少的排列顺序是C>B>A>D>E;
故答案为:C>B>A>D>E;
(2)量筒的刻度由上到下逐渐减小,用量筒量取一定体积的液体时,若采用俯视的方法量取20ml液体,俯视时液面低于刻度线,所以实际量取的液体的体积比20ml小,量筒中实际有20ml液体,而你读数时采用了俯视的方法,俯视时液面低于刻度线,则读得的数据比20ml大,
故答案为:小;大;
(3)由题意可知,硫酸与氯化钡反应的方程式为:BaCl2+H2SO4═BaSO4↓+2HCl,由方程式可知:硫酸与硫酸钡的质量关系为98:233,由于产生沉淀的质量和原硫酸溶液的质量相等,所以原硫酸溶液中溶质的质量分数为:
×100%=42.06%.
故答案为:42.06%.
B.所含电子的物质的量为4mol的H2物质的量为2mol;
C.20℃45g H2O物质的量为2.5mol;
D.常温下,16g O2与14g N2的混合气体,物质的量为1mol;
E.含原子总数约为1.204×1024的NH3,物质的量为0.25mol;
则物质所含分子数由多到少的排列顺序是C>B>A>D>E;
故答案为:C>B>A>D>E;
(2)量筒的刻度由上到下逐渐减小,用量筒量取一定体积的液体时,若采用俯视的方法量取20ml液体,俯视时液面低于刻度线,所以实际量取的液体的体积比20ml小,量筒中实际有20ml液体,而你读数时采用了俯视的方法,俯视时液面低于刻度线,则读得的数据比20ml大,
故答案为:小;大;
(3)由题意可知,硫酸与氯化钡反应的方程式为:BaCl2+H2SO4═BaSO4↓+2HCl,由方程式可知:硫酸与硫酸钡的质量关系为98:233,由于产生沉淀的质量和原硫酸溶液的质量相等,所以原硫酸溶液中溶质的质量分数为:
| 98 |
| 233 |
故答案为:42.06%.
点评:本题考查物质的量的相关计算、量筒的使用、溶液质量分数的计算等,题目难度中等,注意有关计算公式的运用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
以下说法正确的是( )
| A、同周期的ⅡA族与ⅢA族的原子序数差只相差1 |
| B、第五周期所能容纳的元素种类有32种 |
| C、第十四列元素所在的族是第ⅣA族 |
| D、118号元素预测是金属 |
容量瓶上需标a.温度 b.浓度 c.容量 d.压强 e.刻度线中的( )
| A、a、c、e |
| B、c、d、e |
| C、a、b、d |
| D、b、c、d |
下列反应的离子方程式中,不正确的是( )
| A、碳酸钠溶液中加入氯化钙溶液:Ca2++CO32-═CaCO3↓ |
| B、实验室用石灰石制取CO2:CO32-2H+═H2O+CO2↑ |
| C、碳酸氢钙溶液跟盐酸反应:Ca2++2HCO3-+2H+═Ca2++2H2O+2CO2↑ |
| D、醋酸跟氢氧化钾溶液反应:CH3COOH+OH-═CH3COO-+H2O |
常温下,下列各组离子加入Na2O2后仍能大量共存的是( )
| A、H+、Fe2+、Cl-、SO42- |
| B、K+、SiO32-、Cl-、NO3- |
| C、Na+、K+、NH4+、NO3- |
| D、Cl-、NO3-、Na+、SO32- |
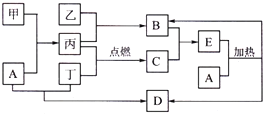
 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石 油化工发展水平,A还是一 种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据如图回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石 油化工发展水平,A还是一 种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.根据如图回答下列问题: