题目内容
7.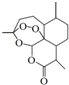 青蒿素是从植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯药物.其结构简式如图所示,则下列关于青蒿素的叙述正确的是( )
青蒿素是从植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯药物.其结构简式如图所示,则下列关于青蒿素的叙述正确的是( )| A. | 青蒿素易溶于水,难溶于乙醇和丙酮等溶剂 | |
| B. | 青蒿素的分子式为:C15H20O5 | |
| C. | 青蒿素因其具有“-O-O-”,所以具有一定的氧化性 | |
| D. | 青蒿素可以与NaOH、Na2CO3、NaHCO3发生反应 |
分析 由结构简式可知分子式,分子中含-COOC-及-C-O-C-、-O-O-,结合酯、醚及过氧化物的性质来解答.
解答 解:A.含有酯基,难溶于水,易溶于乙醇、丙酮等溶剂,故A错误;
B.由结构简式可知,青蒿素的化学式为C15H22O5,故B错误;
C.由过氧化物的性质可知,青蒿素中含有过氧键-O-O-,一定条件下其可能具有较强的氧化性,故C正确;
D.含有酯基,不含羧基,与碳酸氢钠不反应,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型,把握官能团与性质的关系,熟悉酯的性质即可解答,注意知识的迁移应用,题目难度不大.

练习册系列答案
相关题目
17.下列关于电解质电离的叙述中,不正确的是( )
| A. | 电解质的电离过程就是产生自由移动离子的过程 | |
| B. | 碳酸钙在水中难溶,但被溶解的碳酸钙全部电离,所以碳酸钙是强电解质 | |
| C. | 氯气和氨气的水溶液导电性都很好,所以它们是强电解质 | |
| D. | 水难电离,纯水几乎不导电,所以水是弱电解质 |
18.下列说法正确的是( )
| A. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| B. | 新制氯水中的所有物质都是电解质 | |
| C. | 氮氧化物、二氧化硫是形成酸雨的主要物质 | |
| D. | 制造光导纤维的原料是晶体硅 |
15.下列有关有机化学的说法中正确的是( )
| A. | 除去硬脂酸钠溶液中的甘油方法是:往溶液中加入饱和食盐水,分液 | |
| B. | 治疗疟疾的青蒿素(如图)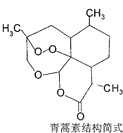 ,分子式是C15H20O5 ,分子式是C15H20O5 | |
| C. | 有机物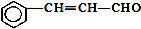 可发生加成反应、氧化反应、还原反应和聚合反应 可发生加成反应、氧化反应、还原反应和聚合反应 | |
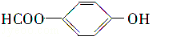
| D. | 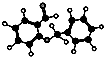 右图所示的有机物分子式为C14H12O2,不能发生银镜反应 右图所示的有机物分子式为C14H12O2,不能发生银镜反应 |
2.下列说法正确的是( )
| A. | 离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | |
| B. | 往海带灰的浸泡液中加入过量的氯水,保证I-完全氧化为I2 | |
| C. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| D. | 等质量的甲醛与乳酸[CH3CH(OH)COOH]完全燃烧消耗氧气的量不相等 |
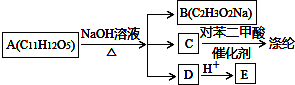
12. 如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述一定正确的是( )
如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述一定正确的是( )
 如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述一定正确的是( )
如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述一定正确的是( )| A. | 反应①属于加成反应 | B. | 1molZ完全加成需要3molH2 | ||
| C. | X与W属于同系物 | D. | X、Y、Z、W都能与NaOH溶液反应 |
16.某学生用化学知识解决生活中的问题,下列家庭小实验或说法不合理的是( )
| A. | 用米汤检验食盐中是否含碘酸钾(KIO3) | |
| B. | 用食醋除去暖水瓶中的薄层水垢 | |
| C. | 医用酒精的浓度通常为75%,可用于杀菌消毒 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物 |
6.镍电池广泛应用于混合动力汽车系统,电极材料由NiO2、Fe和碳粉涂在铝箔上制成.放电过程中产生Ni(OH)2和Fe(OH)2,Fe(OH)2最终氧化、脱水生成氧化铁.由于电池使用后电极材料对环境有危害,某学习小组对该电池电极材料进行回收研究.
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+.
②某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
回答下列问题:
(1)该电池的负极材料是Fe正极反应式为NiO2+2H2O+2e-=Ni(OH)2+2OH-;
(2)若电池输出电压为3V,给2W灯泡供电,当电池消耗0.02gFe,理论上电池工作1.72min(小数点后保留2位),(已知F=96500C/mol)
(3)将电池电极材料用盐酸溶解后加入适量双氧水,其目的是将溶液中的Fe2+氧化为Fe3+,过滤,在滤液中个慢慢加入NiO固体,则开始析出沉淀时的离子方程式是NiO+2H+=Ni2++H2O和Fe3++3H2O=Fe(OH)3↓+3H+.若将两种杂质阳离子都沉淀析出,pH应控制在5.1~5.9之间(离子浓度小于或等于1×10-5mol/L为完全沉淀,lg2=0.3、lg3=0.5);设计将析出的沉淀混合物中的两种物质分离开来的实验方案将混合物加入NaOH溶液中充分溶解,过滤、洗涤,滤渣为Fe(OH)3,将滤液通入足量CO2,过滤、洗涤,得沉淀物Al(OH)3
(4)将加入NiO过滤后的溶液加入Na2C2O4,得到NiC2O4•2H2O和滤液A,A的主要成分是NaCl溶液;电解滤液A,在阴极产生气体BH2(填分子式);在阳极产生气体CCl2(填分子式).将NiC2O4•2H2O加入到电解后的溶液,再通入电解时某电解产生的气体,即可得到回收产品Ni(OH)3,所通入气体为C(填“B”、“C”)极气体,判断依据是要实现Ni(OH)2→Ni(OH)3,镍元素化合价升高,需要加入氧化剂,则通入的气体应为阳极产生的Cl2.
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+.
②某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 2.0×10-32 | 3.8 | - |
| Fe(OH)3 | 4.0×10-38 | 1.9 | 3.2 |
| Fe(OH)2 | 8.0×10-15 | 6.95 | 9.95 |
| Ni(OH)2 | 6.5×10-18 | 5.9 | 8.9 |
(1)该电池的负极材料是Fe正极反应式为NiO2+2H2O+2e-=Ni(OH)2+2OH-;
(2)若电池输出电压为3V,给2W灯泡供电,当电池消耗0.02gFe,理论上电池工作1.72min(小数点后保留2位),(已知F=96500C/mol)
(3)将电池电极材料用盐酸溶解后加入适量双氧水,其目的是将溶液中的Fe2+氧化为Fe3+,过滤,在滤液中个慢慢加入NiO固体,则开始析出沉淀时的离子方程式是NiO+2H+=Ni2++H2O和Fe3++3H2O=Fe(OH)3↓+3H+.若将两种杂质阳离子都沉淀析出,pH应控制在5.1~5.9之间(离子浓度小于或等于1×10-5mol/L为完全沉淀,lg2=0.3、lg3=0.5);设计将析出的沉淀混合物中的两种物质分离开来的实验方案将混合物加入NaOH溶液中充分溶解,过滤、洗涤,滤渣为Fe(OH)3,将滤液通入足量CO2,过滤、洗涤,得沉淀物Al(OH)3
(4)将加入NiO过滤后的溶液加入Na2C2O4,得到NiC2O4•2H2O和滤液A,A的主要成分是NaCl溶液;电解滤液A,在阴极产生气体BH2(填分子式);在阳极产生气体CCl2(填分子式).将NiC2O4•2H2O加入到电解后的溶液,再通入电解时某电解产生的气体,即可得到回收产品Ni(OH)3,所通入气体为C(填“B”、“C”)极气体,判断依据是要实现Ni(OH)2→Ni(OH)3,镍元素化合价升高,需要加入氧化剂,则通入的气体应为阳极产生的Cl2.


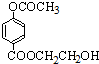 或
或