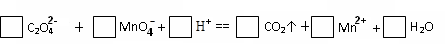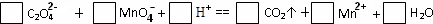题目内容
(1) 配平以下氧化还原反应方程式:
![]()
当KMnO4消耗0.05 mol时,产生的CO2的体积为 L(标准状况)。
(2) 家用液化气中主要成份之一是丁烷,当10 kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量5×105 kJ,试写出丁烷燃烧反应的热化学方程式:
已知1 mol液态水气化时需要吸收44 kJ热量,则1 mol丁烷完全燃烧产生气态水时放出的热为 kJ。
(1) 5,2,3—10,1,2,8; 5.6
(2) C4H10(g)+6.5O2(g) = 4CO2(g)+5H2O(l) △H=-2900 kJ·mol-1
或2C4H10(g)+13O2(g) = 8CO2(g)+10H2O(l) △H=-5800 kJ·mol-1
2680

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
 H++C2O42-
H++C2O42-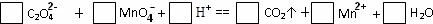
 4分)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。
4分)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。 L 0.01 mol/L NaHC2O4溶液中滴加10mL 0.01 mol/L NaOH溶液时,比较溶液中各种离子浓度的大小关系,用>连接: ;
L 0.01 mol/L NaHC2O4溶液中滴加10mL 0.01 mol/L NaOH溶液时,比较溶液中各种离子浓度的大小关系,用>连接: ;