题目内容
下列叙述中正确的是( )
| A、能电离出氢离子的化合物叫做酸 |
| B、能电离出氢氧根离子的化合物叫做碱 |
| C、能电离出酸根离子的化合物叫做盐 |
| D、由金属离子(或铵根离子)和酸根离子组成的化合物属于盐 |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:A、酸是电离出的阳离子全部是氢离子的化合物;
B、碱是电离出的阴离子全部是氢氧根的化合物;
C、盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物;
D、盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物.
B、碱是电离出的阴离子全部是氢氧根的化合物;
C、盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物;
D、盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物.
解答:
解:A、电离出的阳离子全部是氢离子的化合物是酸,故A错误;
B、电离出的阴离子全部是氢氧根的化合物是碱,故B错误;
C、阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物是盐,故C错误;
D、阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物是盐,故D正确.
故选D.
B、电离出的阴离子全部是氢氧根的化合物是碱,故B错误;
C、阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物是盐,故C错误;
D、阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物是盐,故D正确.
故选D.
点评:本题考查了酸碱盐的概念,难度不大,属于基础型题目.

练习册系列答案
相关题目
下列离子组在指定溶液中能大量共存的是( )
| A、能使甲基橙呈红色的溶液中:K+、Fe2+、NO3-、SO42- | ||
| B、滴加酚酞试液显红色的溶液中:Ag+、NH4+、Cl-、SO32- | ||
| C、常温下pH=12的溶液中:K+、Na+、CO32-、NO3- | ||
D、常温下
|
强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ?mol-1.
分别向1L0.5mol?L-1的Ba(OH)2的溶液中加入①浓硫酸、②稀硫酸、③稀硝酸、④稀醋酸恰好完全反应的热效应分别为△H1、△H2、△H3、△H4,下列关系正确的是( )
分别向1L0.5mol?L-1的Ba(OH)2的溶液中加入①浓硫酸、②稀硫酸、③稀硝酸、④稀醋酸恰好完全反应的热效应分别为△H1、△H2、△H3、△H4,下列关系正确的是( )
| A、△H1>△H2>△H3>△H4 |
| B、△H1<△H2<△H3<△H4 |
| C、△H1>△H2=△H3>△H4 |
| D、△H4<△H1=△H2<△H3 |
两瓶体积相等的气体,一瓶是NO,另一瓶是N2和O2,同温同压时瓶内气体的关系一定正确的是( )
| A、所含原子数相等 |
| B、气体密度相等 |
| C、气体质量相等 |
| D、摩尔质量相等 |
下列叙述正确的是( )
| A、“绿色食物”就是指绿色的食物 |
| B、离子键、共价键和氢键都是化学键 |
| C、任何化学反应都伴随有能量的变化 |
| D、溶于水后能电离出H+的化合物就是酸 |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,2.24L水中所含的电子数为NA |
| B、常温常压下,16g O3所含的原子数为NA |
| C、0.1molNa2O2晶体中所含的离子数为0.4NA |
| D、1molFe在氧气中充分燃烧失去的电子数为3NA |
下列化学用语错误的是( )
A、氟离子的结构示意图: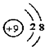 |
B、-CH3的电子式: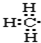 |
C、Na+的电子排布图: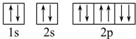 |
| D、Na的简化电子排布式:[Ne]3s1 |