题目内容
12.根据等电子规则.下列分子或离子与硫酸根离子又相似结构的是( )| A. | PCl5 | B. | CCl4 | C. | NF3 | D. | N2 |
分析 具有相同原子数和价电子数的微粒互称为等电子体.它们具有相似的结构特征,据此分析解答.
解答 解:原子个数相等、价电子数相等的微粒互为等电子体,等电子体的结构相似,SO42-中原子个数是5、价电子数是32,
A.PCl5中原子个数是6、价电子数是40,所以与硫酸根离子不是等电子体,其结构不同,故A错误;
B.CCl4中原子个数是5、价电子数是32,所以与硫酸根离子是等电子体,其结构相似,故B正确;
C.NF3中原子个数是5、价电子数是26,所以与硫酸根离子不是等电子体,其结构不同,故C错误;
D.N2中原子个数是2、价电子数是14,所以与硫酸根离子不是等电子体,其结构不同,故D错误;
故选B.
点评 本题以硫酸根离子为载体考查等电子体、微粒空间构型,侧重考查等电子体概念及其性质,题目难度不大.

练习册系列答案
相关题目
2. 已知[Co(NH3)6]3+呈正八面体结构(如图):各NH3分子间距相等,Co3+位于正八面的中心.若其中2个NH3分子被Cl-取代,所形成的[Co(NH3)4Cl2]+的同分异构体的种数有( )
已知[Co(NH3)6]3+呈正八面体结构(如图):各NH3分子间距相等,Co3+位于正八面的中心.若其中2个NH3分子被Cl-取代,所形成的[Co(NH3)4Cl2]+的同分异构体的种数有( )
 已知[Co(NH3)6]3+呈正八面体结构(如图):各NH3分子间距相等,Co3+位于正八面的中心.若其中2个NH3分子被Cl-取代,所形成的[Co(NH3)4Cl2]+的同分异构体的种数有( )
已知[Co(NH3)6]3+呈正八面体结构(如图):各NH3分子间距相等,Co3+位于正八面的中心.若其中2个NH3分子被Cl-取代,所形成的[Co(NH3)4Cl2]+的同分异构体的种数有( )| A. | 2 种 | B. | 4种 | C. | 6种 | D. | 1种 |
3.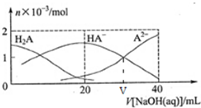 25℃下,向20mL0.1mol/LH2A溶液中滴加0.1mol/LNaOH 溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL0.1mol/LH2A溶液中滴加0.1mol/LNaOH 溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
 25℃下,向20mL0.1mol/LH2A溶液中滴加0.1mol/LNaOH 溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL0.1mol/LH2A溶液中滴加0.1mol/LNaOH 溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )| A. | H2A 电离方程式 H2A═2H++A2- | |
| B. | V[NaOH(aq)]=20mL 时,溶液显碱性 | |
| C. | 已知25℃时 K2(H2A)=1.0×10-9.1,则V[NaOH(aq)]=VmL 时,pH=9.1 | |
| D. | V[NaOH(aq)]=20mL时时,溶液中存在关系:(HA-)+C(A2-)+C(H2A)=0.1mol/L |
20.某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是( )
| A. | 分子中的C、H、O的个数比为1:2:3 | |
| B. | 分子中C、H个数比为1:2 | |
| C. | 该有机物的相对分子质量为14的倍数 | |
| D. | 该分子中肯定不含氧元素 |
7.分子式为C7H5O2Cl的芳香族化合物,结构中含有苯环且能发生银镜反应的共有( )
| A. | 8种 | B. | 10种 | C. | 13种 | D. | 16种 |
17.下列说法错误的是( )
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、H+和H2是氢元素的四种不同粒子 | |
| B. | 石墨和金刚石互称为同位素 | |
| C. | ${\;}_{20}^{40}$Ca和${\;}_{20}^{42}$Ca互称为同位素 | |
| D. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
1.下列物质不属于同素异形体的是( )
| A. | 金刚石和石墨 | B. | 氧气和臭氧 | ||
| C. | 红磷和白磷 | D. | 氢氧化钠和氢氧化钾 |
2.在同温同压下,某有机物和过量Na反应得到V1L氢气,另一份等质量的有机物和足量的NaHCO3反应得到V2L二氧化碳,若2V1=V2则有机物可能是( )
| A. |  | B. | HOOC-COOH | C. | HOCH2CH2OH | D. |  |