题目内容
 红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g),反应过程和能量关系如图所示(图中的△H表示生成 l mol 产物的数据).
红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g),反应过程和能量关系如图所示(图中的△H表示生成 l mol 产物的数据).根据如图回答下列问题:
(1)P和Cl2反应生成PC13的热化学方程式是
(2)PC15分解成 PC13和Cl2的热化学方程式是
考点:反应热和焓变,热化学方程式
专题:化学反应中的能量变化
分析:(1)根据图象及反应热知识分析;依据书写热化学方程式的原则书写;
(2)根据热化学反应方程式的书写原则及化学平衡知识分析;
(2)根据热化学反应方程式的书写原则及化学平衡知识分析;
解答:
解:(1)热化学方程式书写要求:注明各物质的聚集状态,判断放热反应还是吸热反应,反应物的物质的量与反应热成对应的比例关系,根据图示P(s)+32Cl2(g)→PCl3(g),反应物的总能量大于生成物的总能量,该反应是放热反应,反应热为△H=-306 kJ/mol,热化学方程式为:P(s)+32Cl2(g)═PCl3(g);△H=-306 kJ/mol,
故答案为:P(s)+
Cl2(g)═PCl3(g);△H=-306kJ?mol-1;
(2)△H=生成物总能量-反应物总能量,Cl2(g)+PCl3(g)=PCl5(g),中间产物的总能量大于最终产物的总能量,该反应是放热反应,所以 PCl5(g)=PCl3(g)+Cl2(g)是吸热反应;热化学方程式:PCl5(g)=PCl3(g)+Cl2(g);△H=+93 kJ/mol;
故答案为:PCl5(g)=PCl3(g)+Cl2(g);△H=+93 kJ/mol;
故答案为:P(s)+
| 1 |
| 2 |
(2)△H=生成物总能量-反应物总能量,Cl2(g)+PCl3(g)=PCl5(g),中间产物的总能量大于最终产物的总能量,该反应是放热反应,所以 PCl5(g)=PCl3(g)+Cl2(g)是吸热反应;热化学方程式:PCl5(g)=PCl3(g)+Cl2(g);△H=+93 kJ/mol;
故答案为:PCl5(g)=PCl3(g)+Cl2(g);△H=+93 kJ/mol;
点评:本题通过图象书写热化学方程式,注意分析图象,题目难度中等.

练习册系列答案
相关题目
列有关实验原理、装置、操作或结论的描述中,不正确的是(有关装置中的夹持仪器略去未画)( )
A、 制备少量氧气 |
B、 制取二氧化硫、检验二氧化硫的漂白性 |
C、 检查装置的气密性 |
D、 实验室用乙醇和浓硫酸制乙烯 |
已知乙烯醇(CH2=CH-OH)不稳定,会自动转化为乙醛,据此推测乙二醇(HOCH2CH2OH)在一定条件下发生脱水反应所得产物可能有( )
①CH3CH2OH ② ③CH3CHO ④
③CH3CHO ④ ⑤
⑤ ⑥CH2=CH2.
⑥CH2=CH2.
①CH3CH2OH ②
 ③CH3CHO ④
③CH3CHO ④ ⑤
⑤ ⑥CH2=CH2.
⑥CH2=CH2.| A、②③④⑤ |
| B、①②③④⑤⑥ |
| C、②③④⑤⑥ |
| D、①②③④⑤ |
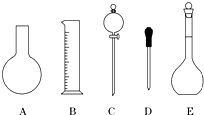 实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题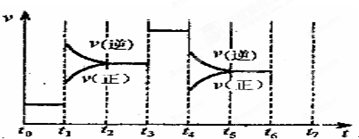
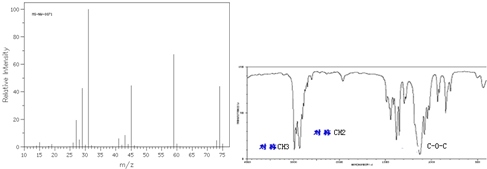
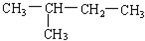 (8)
(8)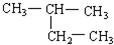 (9)新戊烷.
(9)新戊烷.