题目内容
化学与生活密切相关,下列有关说法正确的是( )
| A、目前加碘食盐中主要添加的是KI |
| B、生理盐水的浓度为0.9% |
| C、淀粉、蛋白质、脂肪都是营养物质,都属于高分子化合物 |
| D、家庭可以用明矾将自来水净化成纯净水 |
考点:常见的食品添加剂的组成、性质和作用,盐类水解的应用,有机高分子化合物的结构和性质
专题:化学应用
分析:A.加碘食盐中添加的是KIO3;
B.人体血液的“矿化度”(即无机盐的相对含量)为0.9%;
C.相对分子质量在10000以上的有机化合物为高分子化合物;
D.明矾只能除去水中悬浮的杂质.
B.人体血液的“矿化度”(即无机盐的相对含量)为0.9%;
C.相对分子质量在10000以上的有机化合物为高分子化合物;
D.明矾只能除去水中悬浮的杂质.
解答:
解:A.目前加碘食盐中主要添加的是KIO3,故A错误;
B.生理盐水的浓度(即无机盐的相对含量)为0.9%,故B正确;
C.油脂相对分子质量较小,不属于高分子化合物,故C错误;
D.明矾只能除去水中悬浮的杂质,不能除去水中的离子,故D错误.
故选B.
B.生理盐水的浓度(即无机盐的相对含量)为0.9%,故B正确;
C.油脂相对分子质量较小,不属于高分子化合物,故C错误;
D.明矾只能除去水中悬浮的杂质,不能除去水中的离子,故D错误.
故选B.
点评:本题考查化学与生活,涉及碘盐、生理盐水、高分子化合物以及明矾净水,注意掌握明矾净水的原理,难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
一定条件下,在反应:2SO2(g)+O2(g)?2SO3(g)的化学平衡体系中,SO2、O2、SO3的浓度分别为2mol?L-1、0.8mol?L-1、2.4mol?L-1,则O2在反应起始时可能的浓度范围是( )
| A、0.8~2.0 mol?L-1 |
| B、0~2.0 mol?L-1 |
| C、0~0.8 mol?L-1 |
| D、无法确定 |
下列可逆反应一定处于平衡状态的是( )
| A、2HBr(g)?Br2 (g)+H2 (g),固定反应容器中压强不再改变. |
| B、N2(g)+3H2 (g)?2 NH3 (g) 测得正反应速率υ(N2)=0.01 mol?L-1?min-1,逆反应速率υ,(NH3 )=0.01 mol?L-1?mⅠn-1 |
| C、2SO2 (g)+O2 (g)?2SO3(g),在 t1和t2 时刻SO2 的转化率为 40% |
| D、2CO(g)+O2(g)?2CO2(g),测得混合物中CO、O2和CO2的物质的量之比为 2:1:1 |
配制100mL0.100mol/LNaOH溶液时,下列操作造成浓度偏高的是①在纸上称量 ②没有冲洗玻璃棒和烧杯2-3次 ③定容时俯视刻度线 ④转移时有少量溶液溅出( )
| A、③ | B、①②③ | C、①②④ | D、②③ |
下列有关说法正确的是( )
| A、放热反应在任何条件都能自发进行 |
| B、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C、任何能使熵值增大的过程都能自发进行 |
| D、△H>0,△S<0的化学反应一定能自发进行 |
氨能跟氧气在铂催化下反应生成硝酸和水,其中第一步反应为:4NH3+5O2═4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(H2O)[mol?L-1?min-1]表示,则正确的关系是( )
| A、4v(NH3)=5v(O2) |
| B、5v(O2)=6v(H2O) |
| C、2v(NH3)=3v(H2O) |
| D、4v(O2)=5v(NO) |
关于如图所示各装置的叙述中,正确的是( )
A、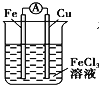 是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
B、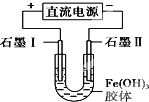 通电一段时间后石墨Ⅱ电极附近溶液红褐色加深 |
C、若用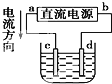 精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
D、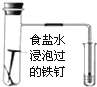 研究的是金属的析氢腐蚀,Fe上的反应为Fe-2e-=Fe2+ |
设NA代表阿伏加德罗常数的数值,下列说法不正确的是( )
| A、36g镁在足量的二氧化碳气体中完全燃烧共转移的电子数为3NA |
| B、1L 1mol?L-1的Na2CO3溶液中含有Na+的数目为NA |
| C、标准状况下,2.24L CO2和SO2混合气体中含有的氧原子数目为0.2NA |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |