题目内容
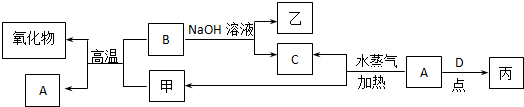
t℃时,将6molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(气)+B(气)?xC(气),2min时反应达到平衡状态(温度不变),剩余1.6molB,并测得C的浓度为0.8mol/L,请填写下列空白:
(1)x= ;
(2)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是
(选填字母)
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率将发生同等程度的改变
(3)若向原平衡混合物的容器中再充入2a molC,在t℃时达到新的平衡,此时B的物质的量为n(B)= mol (用含a的式子表示)
(4)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为 .
(1)x=
(2)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率将发生同等程度的改变
(3)若向原平衡混合物的容器中再充入2a molC,在t℃时达到新的平衡,此时B的物质的量为n(B)=
(4)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为
考点:化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:(1)依据平衡三段式列式计算,平衡常数等于生成物平衡浓度的幂次方乘积除以反应物平衡浓度的幂次方乘积;
(2)恒温恒容容器中加入氦气是惰性气体,增大体系压强,各气体分压不变,平衡不变;
(3)反应前后气体体积不变,加入C增大压强,平衡不动;反应物的转化率不变,依据(2)计算得到;
(4)依据化学反应达到平衡时“等量等效”的方法分析计算满足的关系.
(2)恒温恒容容器中加入氦气是惰性气体,增大体系压强,各气体分压不变,平衡不变;
(3)反应前后气体体积不变,加入C增大压强,平衡不动;反应物的转化率不变,依据(2)计算得到;
(4)依据化学反应达到平衡时“等量等效”的方法分析计算满足的关系.
解答:
解:(1)t℃时,将3mol A和1mol B气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g)?xC(g),2min时反应达到平衡状态(温度不变),剩余了0.8mol B,并测得C的浓度为0.4mol/L物质的量为0.8mol,
3A(g)+B(g)?xC(g),
起始量(mol) 3 1 0
变化量(mol) 0.6 0.2 0.8
平衡量(mol) 2.4 0.8 0.8
1:x=0.2:0.8=1:4,x=4
故答案为:4;
(2)恒温恒容容器中加入氦气是惰性气体,增大体系压强,各气体分压不变,平衡不变,故答案为:C;
(3)若向原平衡混合物的容器中再充入2a mol C,在t℃时达到新的平衡,反应前后气体体积不变,加入C增大压强,平衡不动;反应物的转化率不变,加入2amolC,相当于AB的起始量为
amol,
amol,依据(2)可知AB的转化率为20%,B反应物质的量
a×20%=0.1amol,生成C0.4amol,则此时B的物质的量为n(B)=1.6+0.4a;
故答案为:1.6+0.4a;
(4)在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C),转化为起始量和原平衡相同;
3A(g)+B(g)?4C(g)
3 1 0
n(A) n(B) n(C)
n(A)+
n(C) n(B)+
n(C) 0
n(A)+
n(C)=6
n(B)+
n(C)=2
n(A)=3n(B),n(C)≥0或n(A)=n(B)=0,n(C)>0,
故答案为:n(A)=3n(B),n(C)≥0或n(A)=n(B)=0,n(C)>0.
3A(g)+B(g)?xC(g),
起始量(mol) 3 1 0
变化量(mol) 0.6 0.2 0.8
平衡量(mol) 2.4 0.8 0.8
1:x=0.2:0.8=1:4,x=4
故答案为:4;
(2)恒温恒容容器中加入氦气是惰性气体,增大体系压强,各气体分压不变,平衡不变,故答案为:C;
(3)若向原平衡混合物的容器中再充入2a mol C,在t℃时达到新的平衡,反应前后气体体积不变,加入C增大压强,平衡不动;反应物的转化率不变,加入2amolC,相当于AB的起始量为
| 3 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:1.6+0.4a;
(4)在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C),转化为起始量和原平衡相同;
3A(g)+B(g)?4C(g)
3 1 0
n(A) n(B) n(C)
n(A)+
| 3 |
| 4 |
| 1 |
| 4 |
n(A)+
| 3 |
| 4 |
n(B)+
| 1 |
| 4 |
n(A)=3n(B),n(C)≥0或n(A)=n(B)=0,n(C)>0,
故答案为:n(A)=3n(B),n(C)≥0或n(A)=n(B)=0,n(C)>0.
点评:本题考查了化学平衡的计算应用,影响平衡因素的理解应用,等效平衡的计算判断,题目难度较大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
化学与生活密切相关,下列有关说法正确的是( )
| A、目前加碘食盐中主要添加的是KI |
| B、生理盐水的浓度为0.9% |
| C、淀粉、蛋白质、脂肪都是营养物质,都属于高分子化合物 |
| D、家庭可以用明矾将自来水净化成纯净水 |
关于电子云的下列说法不正确的是( )
| A、s电子绕核旋转,其轨道为一圆圈,而p电子是走∞字形 |
| B、s轨道都是球形轨道 |
| C、轨道不同,电子云的取向不一样 |
| D、电子云图是形象地描述电子在空间单位体积内出现概率大小的图形 |
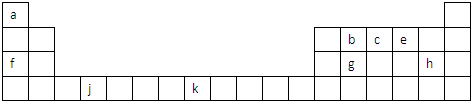
 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图.下列说法正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图.下列说法正确的是( )| A、元素Y与元素Z的最高正化合价之和的数值等于9 |
| B、离子Y2-和Z3+的核外电子数和电子层数都不相同 |
| C、原子半径的大小顺序为:rZ>rW>rQ>rX>rY |
| D、元素W的氢化物稳定性和还原性均比Q的强 |