��Ŀ����
�����14�֣�
���ж��ֺ����ᣬ�����ᣨH2SO3�������ᣨH2SO4���������ᣨH2SO4��SO3����������ᣨH2S2O3���ȵȣ�����������Ϊ��Ҫ���ڹ�ҵ���й㷺��Ӧ�á���ʵ���ң�Ũ�����dz��õĸ������
������м��㣺
(1)�����ᣨH2SO4��SO3������ˮ�����е�SO3��ת��Ϊ���ᡣ����445g����������ˮ���4.00L���ᣬ����������ʵ���Ũ��Ϊ________mol/��
(2)����Ũ������ˮ�����ɵ�H2SO4��H2O���㣬250g��������Ϊ98%�����������ն���gˮ��
(3)�������ǹ�ҵ�����������Ҫԭ�ϡ��������������յĻ�ѧ��Ӧ���£�
3FeS2��8O2��Fe3O4��6SO2 4FeS2��11 O2��2Fe2O3��8SO2
��48mol FeS2��ȫ��Ӧ��������2934.4L����״���������㷴Ӧ������Fe3O4��Fe2O3���ʵ���֮�ȡ�
(4)��������ȡ���ᣬ���ܳ��������Դ���ܱ�����������һ�ֺ��з�չǰ;���Ʊ�����ķ�����
�����������Ϊ0.84�Ļ�����壨H2S��H2O��N2���ڿ�������ȫȼ�գ�����������77%���������������SO2���������ˮ�����壩������֪������ɣ�N2�������0.79��O2�������0.21��
(1)1.25 (2)250��98%��98��16��40g
(3)2934.4��22.4��131mol
��Fe3O4 amol Fe2O3 bmol
3a+2b��48 8a+11��2b��131 a��4 b��18
n (Fe3O4):n(Fe2O3)��2:9
(4)������Ϊ1�����0.84���������ȫȼ������0.84������������0.84���ˮ������1.26����������������Ϊ1.26��0.21��1.77��10.62
���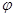 ��0.84�£�10.62��1.26+1.84����0.075
��0.84�£�10.62��1.26+1.84����0.075
�������������(1)445g����������ʵ�����445g��178g/mol��2.5mol����������������������2.5mol��2.5mol���������ֲ���2.5mol���ᣬ����Һ����������ʵ�����5.0mol��Ũ����5.0mol��4L��1.25mol/L��
(2)250g��������Ϊ98%�������������������250g��98%��245g�������ܼ�ˮ��5g����������ʵ�����245g��98g/mol��2.5mol�����Խ��ˮ�����ʵ�����2.5mol��������2.5mol��18g/mol��45g����˻���������ˮ��������45g��5g��40g��
(3)��Fe3O4�����ʵ�����amol��Fe2O3�����ʵ�����bmol
��Ӧ���������������ʵ�����2934.4L��22.4L/mol��131mol
����ݷ���ʽ��֪3a+2b��48��8a+11��2b��131
���a��4��b��18
��n (Fe3O4):n(Fe2O3)��2:9
(4)������Ϊ1����������Ȼ�����ȫȼ�յķ���ʽ2H2S��3O2��ȼ2SO2��2H2O ��֪��0.84���������ȫȼ������0.84������������0.84���ˮ������1.26�����������Ӧ�п�������77%������������Ϊ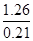 ��1.77��10.62������������������
��1.77��10.62������������������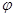 ��
��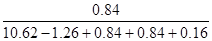 ��0.075
��0.075
���㣺�������仯���ﷴӦ���йػ�ѧ����

̼���仯�����й㷺����;��
��1���ڵ绯ѧ�У�����̼���缫��
��������п�̸ɵ���У�̼���� ����
������̼�����������缫��ⱥ��ʳ��ˮ�����ռ�ʱ��̼���� ������Ӧ�����ӷ���ʽ ��
��2����ˮ����ͨ�����ȵ�̼�ɲ���ˮú����C(s)+H2O(g)  CO(g)+H2(g) ��H=+131.3kJ/mol,�ﵽƽ����������ʱ�������H2O��ƽ��ת���ʵĴ�ʩ�� ��
CO(g)+H2(g) ��H=+131.3kJ/mol,�ﵽƽ����������ʱ�������H2O��ƽ��ת���ʵĴ�ʩ�� ��
| A�������¶� | B������̼������ |
| C��������� | D����CO���ռ���ȥCO |
 CO2(g)+H2(g)�õ��������ݣ�
CO2(g)+H2(g)�õ��������ݣ�| �¶�/�� | ��ʼŨ��mol/L | ƽ��Ũ��mol/L | |
| CO(g) | H2O(g) | H2(g) | |
| 900 | 2.0 | 0.8 | 0.4 |
ͨ�����㣬�÷�Ӧ��ƽ�ⳣ��Ϊ�� ��
��4����ҵ�ϰ�ˮú���еĻ�����崦����ýϴ���H2���ںϳɰ���
N2(g)+3H2(g)һ��������2NH3(g) ��H= ��92.4kJ/molijͬѧ�ڲ�ͬʵ��������ģ�⻯����������ʵ�飬N2Ũ����ʱ��仯��ͼ��
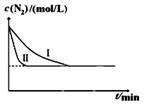
����ʵ��I�Ƚϣ�ʵ��II�ı������Ϊ�� ��
��ʵ��III��ʵ��I���¶�Ҫ�ߣ�����������ͬ��������ͼ����ʵ��I��ʵ��III��NH3Ũ����ʱ��仯��ʾ��ͼ��
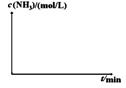
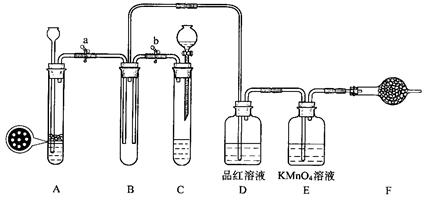
ijС��ͬѧ����ͼװ�ý���ʵ���о�(a��b��c��ʾֹˮ��)�������ۻ������䷽����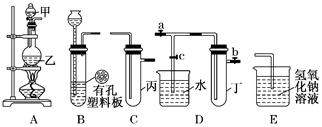
��װ��A��C��E�����ӣ���MnO2��Ũ������ȡ��������ش�
�٣���Ԫ�������ڱ��е�λ��Ϊ ��
�ڣ�A�з�Ӧ�����ӷ���ʽ��___ _��
�ۣ�E������������Һ������__________ ��
��C�м���������ˮ���Ƶ���ˮ����������ˮ�ֳ����ݽ���ʵ�飬�����������ͽ���Ϊ��
| ʵ����� | ʵ����� | ���� | ���� |
| �� | ����ˮ����Ʒ����Һ | Ʒ����Һ��ɫ | ������Ư���� |
| �� | ��ˮ�м���̼�����Ʒ�ĩ | ����ɫ���ݲ��� | ������ˮ��Ӧ�IJ���������� |
�ݣ�ʵ����Ƴ���Ӧ�Ľ����Ƿ������_________��������������˵�����ɣ���������������д��____________________________________ ____________________��
��2�� Ϊ�Ƚ�Cl2��I2��������ǿ������A��C��E������ C��ʢ���Լ�����Ϊ___ _ __��
��3�� ��B��D��E��������B��װŨ�����ͭƬ�����Ƶ�NO2�������й�ʵ�飮
��.B�з�Ӧ�Ļ�ѧ����ʽ_____________________ ______ __________��
��.�����ر�c�������г�������ɫ��NO2ʱ���ٹر�ֹˮ��a��b�����Թܶ�, ���пɹ۲쵽��ʵ������ ��

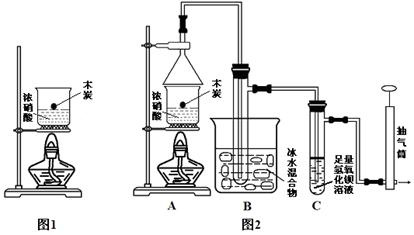
 ��ij��ѧ��ȤС��ģ��ô������̵�ʵ��װ�����£��г�װ������ȥ����
��ij��ѧ��ȤС��ģ��ô������̵�ʵ��װ�����£��г�װ������ȥ����



 ��������Ϊ����£�SO3������H2O����ʱ�ų�������Ϊ ��������λ��Ч���֣���
��������Ϊ����£�SO3������H2O����ʱ�ų�������Ϊ ��������λ��Ч���֣���