题目内容
【题目】向含有酚酞的NaOH溶液中,逐滴滴入新制氯水,边滴边振荡,并连续观察现象,发现溶液的红色逐渐褪去而得无色溶液。根据预测,实验中溶液红色褪去的原因可能有两种,试回答下列问题:
(1)新制氯水成分:__________________________________________________。
(2)请用简要的文字说明溶液红色褪去的原因可能有两种
①___________________________________________________________________________。
②___________________________________________________________________________。
(3)通过实验进一步探究溶液红色褪去的原因究竟是上述中的①还是②。
a.取试管内的无色溶液3mL盛于另一支洁净的试管中;
b.__________________________________________________________,振荡试管,
(实验现象及结论)
Ⅰ若________________________,则证明溶液红色褪去的原因是①而不是②;
Ⅱ若________________________,则证明溶液红色褪去的原因是②而不是①。
【答案】Cl2、H2O、HClO、H+、Cl-、ClO-、OH- HCl和 HClO中和了NaOH HClO氧化了酚酞 再向褪色后试管内滴加几滴NaOH溶液 恢复红色 仍为无色
【解析】
(1)Cl2+H2O![]() HCl+HClO,盐酸可完全电离,HClO存在电离平衡;
HCl+HClO,盐酸可完全电离,HClO存在电离平衡;
(2)HCl、HClO与NaOH反应使碱性降低,或HClO氧化酚酞,均可能使溶液褪色;
(3)若继续加碱,溶液变红,为中和反应导致褪色;若继续加碱,溶液不变红,为HClO氧化酚酞。
(1)Cl2+H2O![]() HCl+HClO,盐酸完全电离,HClO存在电离平衡,则氯水中含微粒为Cl2、H2O、HClO、H+、Cl-、ClO-、OH-;
HCl+HClO,盐酸完全电离,HClO存在电离平衡,则氯水中含微粒为Cl2、H2O、HClO、H+、Cl-、ClO-、OH-;
(2)因碱遇酚酞变红,氯水中有盐酸、HClO,均与碱发生中和反应,碱性降低,则红色褪去,氯水中还有次氯酸,次氯酸具有强氧化性,HClO氧化了酚酞而使红色褪色,溶液红色褪去的原因可能有两种为HCl和HClO中和了NaOH、HClO氧化了酚酞;
(3)对褪色的溶液,取试管内的无色溶液3mL盛于另一支洁净的试管中,再向试管内滴加2滴NaOH溶液振荡后发现恢复红色,则证明溶液红色褪去的原因是①而不是②;若再加碱,仍为无色,则证明溶液红色褪去的原因是②而不是①。

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】氢原子是最轻的原子,人们曾预言它可能是所有元素之母。学习物质结构与性质,回答下列问题:
(1)太阳中的主要化学元素是氢和_______。
(2)氢负离子H-基态电子排布式为_______。
(3)下列变化:H-(g)=H(g)+e-吸收的能量为73kJ/mol,H(g)=H+(g)+e-吸收的能量为1311kJ/mol,则氢负离子H-的第一电离能为________。
(4)几种碱金属氢化物的部分性质如下表所示:
氢化物 | LiH | NaH | KH |
密度/g/cm3 | 0.78 | 1.43 | |
分解温度/℃ | 850 | 425 | 400 |
从化学结构的角度回答说明,分解温度LiH>NaH>KH___。
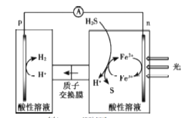
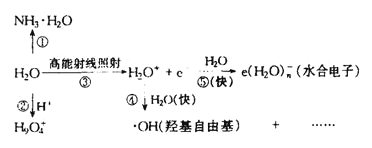
(5)水溶液中有H3O+、H5O2+、H9O4+等微粒的形式。H3O+中,中心原子的杂化类型是___,请画出H5O2+的结构式:______。当用高能射线照射液态水时,水分子便以一种新的方式电离,如图所示写出高能射线照射水的总反应的离子方程式_______。
(6)氢化铝钠(NaAlH4)等复合氢化物是重要的有机还原剂。NaAlH4晶胞结构如图所示,NaAlH4晶体中,与Na+紧邻且等距的A1H4-有___个,设阿伏伽德罗常数为NA,则晶体的密度为___g·cm-3。
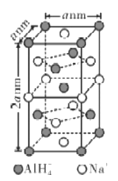
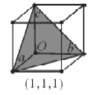
(7)在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为(1,1,1)晶面。如图则该立方晶胞体中(1,1,1)晶面共有___个。