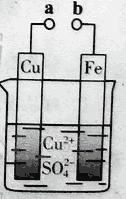
ЬтФПФкШн
ЁОЬтФПЁПЛЏКЯЮяNОпгаеђЭДЁЂЯћбзЕШвЉРэзїгУЃЌЦфКЯГЩТЗЯпШчЯТЃК
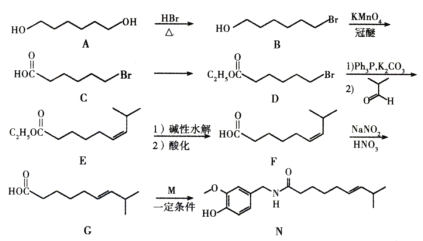
(1)AЕФЯЕЭГУќУћЮЊ____________ЃЌEжаЙйФмЭХЕФУћГЦЮЊ_____________ЁЃ
(2)AЁњBЕФЗДгІРраЭЮЊ____________ЃЌДгЗДгІЫљЕУвКЬЌгаЛњЛьКЯЮяжаЬсДПBЕФГЃгУЗНЗЈЮЊ_____________ЁЃ
(3)CЁњDЕФЕФЛЏбЇЗНГЬЪНЮЊ_____________ЁЃ
(4)CЕФЭЌЗжвьЙЙЬхW(ВЛПМТЧЪжадвьЙЙ)ПЩЗЂЩњвјОЕЗДгІЃЛЧв1 mol WзюЖргы2 mol NaOHЗЂЩњЗДгІЃЌВњЮяжЎвЛПЩБЛбѕЛЏГЩЖўдЊШЉЁЃТњзуЩЯЪіЬѕМўЕФWга____________жжЃЌШєWЕФКЫДХЙВеёЧтЦзОпгаЫФзщЗхЃЌдђЦфНсЙЙМђЪНЮЊ_____________ЁЃ
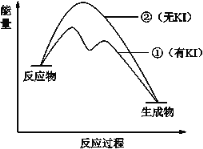
(5)ВЮееЩЯЪіКЯГЩТЗЯпЃЌвд![]() ЮЊдСЯЃЌВЩгУШчЯТЗНЗЈжЦБИвНвЉжаМфЬх
ЮЊдСЯЃЌВЩгУШчЯТЗНЗЈжЦБИвНвЉжаМфЬх![]() ЁЃ
ЁЃ
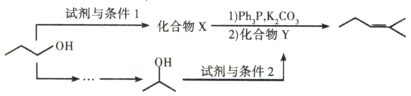
ИУТЗЯпжаЪдМСЬѕМў1ЮЊ____________ЃЌXЕФНсЙЙМђЪНЮЊ____________ЃЛЪдМСгыЬѕМў2ЮЊ____________ЃЌYЕФНсЙЙМђЪНЮЊ_____________ЁЃ
ЁОД№АИЁП1ЃЌ6-МКЖўДМ ѕЅЛљКЭЬМЬМЫЋМќ ШЁДњЗДгІ еєСѓ ![]() +C2H5OH
+C2H5OH![]()
![]() +H2O 5
+H2O 5 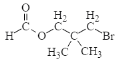 HBrЁЂМгШШ
HBrЁЂМгШШ ![]() O2/CuЛђAgЁЂМгШШ
O2/CuЛђAgЁЂМгШШ ![]()
ЁОНтЮіЁП
AКЭHBrЗЂЩњШЁДњЗДгІЩњГЩBЃЌBЗЂЩњбѕЛЏЗДгІЩњГЩCЃЌИљОнCDНсЙЙМђЪНБфЛЏжЊЃЌCКЭCH3CH2OHЗЂЩњѕЅЛЏЗДгІЩњГЩDЃЌDжафхдзгБЛШЁДњЩњГЩEЃЌEЗЂЩњЫЎНтЗДгІШЛКѓЫсЛЏЕУЕНFЃЌИљОнGЁЂNНсЙЙМђЪНЧјБ№ПЩжЊЃЌGЗЂЩњГЩыФЗДгІЩњГЩNЃЌMНсЙЙМђЪНЮЊ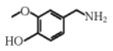 ЁЃ
ЁЃ
(1)AЮЊЖўдЊДМЃЌєЧЛљЗжБ№ЮЛгк1ЁЂ6КХЬМдзгЩЯЃЌAЕФЯЕЭГУќУћЮЊ1ЃЌ6-МКЖўДМЃЛEжаЙйФмЭХЕФУћГЦЮЊѕЅЛљКЭЬМЬМЫЋМќЃЛ
(2)ЖдБШAКЭBЕФНсЙЙПЩжЊЃЌAжаєЧЛљБЛфхдзгДњЬцЩњГЩBЃЌЫљвдЗДгІРраЭЮЊШЁДњЗДгІЃЛЗжРыЛЅШмЕФвКЬЌгаЛњЮяПЩгУеєСѓЕФЗНЗЈЃЛ
(3)CЕНDЮЊCгыввДМЕФѕЅЛЏЗДгІЃЌЗНГЬЪНЮЊ![]() +C2H5OH
+C2H5OH![]()
![]() +H2OЃЛ
+H2OЃЛ
(4)CЮЊ![]() ЃЌЦфЭЌЗжвьЙЙЬхWПЩЗЂЩњвјОЕЗДгІЃЌЫЕУїКЌга-CHOНсЙЙЃЌЧв1mol WзюЖргы2mol NaOHЗЂЩњЗДгІЃЌ1mol-BrПЩгУКЭ1molNaOHЗДгІЃЌдђЛЙгІКЌгаHCOO-(ПЩЗЂЩњвјОЕЗДгІ)ЃЛВњЮяжЎвЛПЩБЛбѕЛЏГЩЖўдЊШЉЃЌЫЕУїѕЅЛљЫЎНтКѓЕФєЧЛљКЭфхдзгЫЎНтЩњГЩЕФєЧЛљдкЭЌвЛЮяжЪжаЃЌЧвгыєЧЛљЯрСЌЕФЬМдзгЩЯгаСНИіЧтдзгЃЌЗћКЯЬѕМўЕФга
ЃЌЦфЭЌЗжвьЙЙЬхWПЩЗЂЩњвјОЕЗДгІЃЌЫЕУїКЌга-CHOНсЙЙЃЌЧв1mol WзюЖргы2mol NaOHЗЂЩњЗДгІЃЌ1mol-BrПЩгУКЭ1molNaOHЗДгІЃЌдђЛЙгІКЌгаHCOO-(ПЩЗЂЩњвјОЕЗДгІ)ЃЛВњЮяжЎвЛПЩБЛбѕЛЏГЩЖўдЊШЉЃЌЫЕУїѕЅЛљЫЎНтКѓЕФєЧЛљКЭфхдзгЫЎНтЩњГЩЕФєЧЛљдкЭЌвЛЮяжЪжаЃЌЧвгыєЧЛљЯрСЌЕФЬМдзгЩЯгаСНИіЧтдзгЃЌЗћКЯЬѕМўЕФга![]() ЁЂ
ЁЂ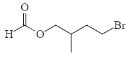 ЁЂ
ЁЂ![]() ЁЂ
ЁЂ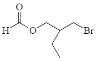 ЁЂ
ЁЂ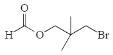 ЃЌЙВ5жжЃЛКЫДХЙВеёЧтжюгаЫФзщЗхЃЌдђЦфНсЙЙМђЪНЮЊ
ЃЌЙВ5жжЃЛКЫДХЙВеёЧтжюгаЫФзщЗхЃЌдђЦфНсЙЙМђЪНЮЊ ЃЛ
ЃЛ
(5)ИљОнXЩњГЩ![]() ЕФЬѕМўЃЌПЩжЊИУЙ§ГЬгыDЕНEЕФЙ§ГЬРрЫЦЃЌЫљвдXжагІКЌгаТБдзгЃЌИљОнAЕНBЕФЗДгІЬѕМўПЩжЊЪдМСгыЬѕМў1ПЩвдЮЊHBrЁЂМгШШЃЌЛЏКЯЮяXЮЊ
ЕФЬѕМўЃЌПЩжЊИУЙ§ГЬгыDЕНEЕФЙ§ГЬРрЫЦЃЌЫљвдXжагІКЌгаТБдзгЃЌИљОнAЕНBЕФЗДгІЬѕМўПЩжЊЪдМСгыЬѕМў1ПЩвдЮЊHBrЁЂМгШШЃЌЛЏКЯЮяXЮЊ![]() ЃЛИљОнDЕНEЕФЗДгІЬѕМўПЩжЊЛЏКЯЮяYжагІКЌгаЬМбѕЫЋМќЃЌдйНсКЯзюжеВњЮяЕФНсЙЙПЩжЊYЮЊ
ЃЛИљОнDЕНEЕФЗДгІЬѕМўПЩжЊЛЏКЯЮяYжагІКЌгаЬМбѕЫЋМќЃЌдйНсКЯзюжеВњЮяЕФНсЙЙПЩжЊYЮЊ![]() ЃЌдђЪдМСгыЬѕМў2ЮЊO2/CuЛђAgЁЂМгШШЁЃ
ЃЌдђЪдМСгыЬѕМў2ЮЊO2/CuЛђAgЁЂМгШШЁЃ

ЁОЬтФПЁПЬММАЦфЛЏКЯЮяЙуЗКДцдкгкздШЛНчЁЃЧыЛиД№ЯТСаЮЪЬтЃК
(1)ЗДгІЂёЃК![]() ЁїH1 ЦНКтГЃЪ§ЮЊK1
ЁїH1 ЦНКтГЃЪ§ЮЊK1
ЗДгІЂђЃК![]() ЁїH2 ЦНКтГЃЪ§ЮЊK2
ЁїH2 ЦНКтГЃЪ§ЮЊK2
ВЛЭЌЮТЖШЯТЃЌK1ЁЂK2ЕФжЕШчЯТБэЃК
| K1 | K2 |
973 | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
ЯжгаЗДгІЂѓЃК![]() ЃЌНсКЯЩЯБэЪ§ОнЃЌЗДгІЂѓЪЧ________ЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉЗДгІЁЃ
ЃЌНсКЯЩЯБэЪ§ОнЃЌЗДгІЂѓЪЧ________ЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉЗДгІЁЃ
(2)![]() ДпЛЏМгЧтКЯГЩЖўМзУбЪЧвЛжж
ДпЛЏМгЧтКЯГЩЖўМзУбЪЧвЛжж![]() зЊЛЏЗНЗЈЃЌЦфЙ§ГЬжажївЊЗЂЩњЯТСаЗДгІЃК
зЊЛЏЗНЗЈЃЌЦфЙ§ГЬжажївЊЗЂЩњЯТСаЗДгІЃК
ЗДгІЂѓЃК![]() ЁїH3
ЁїH3
ЗДгІЂєЃК![]() ЁїH=-122.5kJ/mol
ЁїH=-122.5kJ/mol
дкКубЙЁЂ![]() КЭ
КЭ![]() ЕФЦ№ЪМСПвЛЖЈЕФЬѕМўЯТЃЌ
ЕФЦ№ЪМСПвЛЖЈЕФЬѕМўЯТЃЌ![]() ЦНКтзЊЛЏТЪКЭЦНКтЪБ
ЦНКтзЊЛЏТЪКЭЦНКтЪБ![]() ЕФбЁдёадЫцЮТЖШЕФБфЛЏШчЭМЁЃ
ЕФбЁдёадЫцЮТЖШЕФБфЛЏШчЭМЁЃ
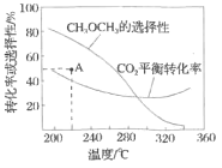
ЦфжаЃК![]() ЕФбЁдёад
ЕФбЁдёад![]()
ЂйЮТЖШИпгк300ЁцЃЌ![]() ЦНКтзЊЛЏТЪЫцЮТЖШЩ§ИпЖјЩЯЩ§ЕФдвђЪЧ________ЁЃ
ЦНКтзЊЛЏТЪЫцЮТЖШЩ§ИпЖјЩЯЩ§ЕФдвђЪЧ________ЁЃ
Ђк220ЁцЪБЃЌдкДпЛЏМСзїгУЯТ![]() гы
гы![]() ЗДгІвЛЖЮЪБМфКѓЃЌВтЕУ
ЗДгІвЛЖЮЪБМфКѓЃЌВтЕУ![]() ЕФбЁдёадЮЊ48%ЃЈЭМжа
ЕФбЁдёадЮЊ48%ЃЈЭМжа![]() ЕуЃЉЁЃВЛИФБфЗДгІЪБМфКЭЮТЖШЃЌвЛЖЈФмЬсИп
ЕуЃЉЁЃВЛИФБфЗДгІЪБМфКЭЮТЖШЃЌвЛЖЈФмЬсИп![]() бЁдёадЕФДыЪЉга________ЁЃ
бЁдёадЕФДыЪЉга________ЁЃ
(3)ЪЏгЭЛЏЙЄЩњВњжаЃЌРћгУСбНтЗДгІПЩвдЛёЕУживЊЛЏЙЄдСЯввЯЉЁЂБћЯЉЁЃвЛЖЈЬѕМўЯТЃЌе§ЖЁЭщСбНтЕФжїЗДгІШчЯТЃК
ЗДгІЂѕЃК![]()
ЗДгІЂіЃК![]()
вЛЖЈЮТЖШЯТЃЌЯђШнЛ§ЮЊ![]() ЕФУмБеШнЦїжаЭЈШые§ЖЁЭщЃЌЗДгІЪБМф
ЕФУмБеШнЦїжаЭЈШые§ЖЁЭщЃЌЗДгІЪБМф![]() гыШнЦїФкЦјЬхзмбЙЧП
гыШнЦїФкЦјЬхзмбЙЧП![]() Ъ§ОнШчЯТЃК
Ъ§ОнШчЯТЃК
| 0 | 10 | 20 | 30 | 40 |
| 5 | 7.2 | 8.4 | 8.8 | 8.8 |
ЂйЗДгІЫйТЪПЩвдгУЕЅЮЛЪБМфФкЗжбЙЕФБфЛЏБэЪОЃЌМДv=![]() ЃЌЧА
ЃЌЧА![]() Фке§ЖЁЭщЕФЦНОљЗДгІЫйТЪvЃЈе§ЖЁЭщЃЉ
Фке§ЖЁЭщЕФЦНОљЗДгІЫйТЪvЃЈе§ЖЁЭщЃЉ![]() ________
________![]() ЃЌИУЮТЖШЯТЃЌе§ЖЁЭщЕФЦНКтзЊЛЏТЪ
ЃЌИУЮТЖШЯТЃЌе§ЖЁЭщЕФЦНКтзЊЛЏТЪ![]() ________ЁЃ
________ЁЃ
ЂкШєЦНКтЪБввЯЉЕФЬхЛ§ЗжЪ§ЮЊ![]() ЃЌдђИУЮТЖШЯТЗДгІЂѕЕФЗжбЙЦНКтГЃЪ§Kp=________MPaЃЈБЃСєвЛЮЛаЁЪ§ЃЉЁЃ
ЃЌдђИУЮТЖШЯТЗДгІЂѕЕФЗжбЙЦНКтГЃЪ§Kp=________MPaЃЈБЃСєвЛЮЛаЁЪ§ЃЉЁЃ
ЂлШєЗДгІдкКуЮТЁЂКубЙЬѕМўЯТНјааЃЌЦНКтКѓЗДгІШнЦїЕФЬхЛ§________![]() ЃЈЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБЃЉЁЃ
ЃЈЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБЃЉЁЃ