题目内容
用20.0g烧碱(NaOH)配制成500mL溶液,其溶质的物质的量浓度为 ;从中取出10mL,这10mL溶液溶质的物质的量浓度是 ,含溶质 g;若将这10mL溶液加水稀释到100mL,所得溶液溶质的物质的量浓度为 ,其中含Na+的物质的量是 .
考点:物质的量浓度的相关计算,溶液的配制
专题:物质的量浓度和溶解度专题
分析:根据n=
计算NaOH物质的量,再根据c=
计算氢氧化钠的物质的量浓度,溶液是均匀的,从中取出的10mL溶液浓度与原溶液浓度相等,根据n=cV计算10mL溶液中n(NaOH),再根据m=nM计算其质量,利用稀释定律计算稀释后氢氧化钠的物质的量浓度,根据n=cV计算钠离子的物质的量.
| m |
| M |
| n |
| V |
解答:
解:20g烧碱的物质的量为:
=0.5mol,则c=
=1mol/L;
溶液为均一的,取出任意体积都和原溶液浓度相等,从中取出10mL溶液,其物质的量浓度为1mol/L,该10mL反应中,溶质的质量为:0.01L×1mol/L×40g/mol=0.4g;
溶液稀释前后溶质的物质的量不变,这10mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为
=0.1mol/L;
其中含Na+的物质的量为:0.1mol/L×0.1L=0.01mol,
故答案为:1mol/L;1mol/L;0.4;0.01mol.
| 20g |
| 40g/mol |
| 0.5mol |
| 0.5L |
溶液为均一的,取出任意体积都和原溶液浓度相等,从中取出10mL溶液,其物质的量浓度为1mol/L,该10mL反应中,溶质的质量为:0.01L×1mol/L×40g/mol=0.4g;
溶液稀释前后溶质的物质的量不变,这10mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为
| 0.01L×1mol/L |
| 0.1L |
其中含Na+的物质的量为:0.1mol/L×0.1L=0.01mol,
故答案为:1mol/L;1mol/L;0.4;0.01mol.
点评:本题考查物质的量浓度有关计算,难度不大,注意有关计算公式的运用,理解溶液的特点以及溶液稀释前后溶质的物质的量不变的特征.

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
下列实验过程中产生的现象与对应的图形正确的是( )
A、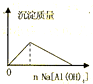 盐酸中加入Na[Al(OH)4]溶液 |
B、 SO2气体通入溴水中 |
C、 向Na2CO3溶液中逐滴滴加盐酸 |
D、 氨水通入醋酸溶液中 |
“五水共治,治污为先”是我省提出改善生态环境的一项重要政策.为了防止水体污染,你认为下列措施中不可行的是( )
| A、不任意排放工业污水 |
| B、禁止使用农药和化肥 |
| C、生活污水经净化处理后再排放 |
| D、牲畜粪便集中处理后再施用 |
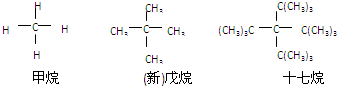 (1)人们在对烷烃分子空间结构的研究中发现某一系列的烷烃分子只有一种一卤代物.如:
(1)人们在对烷烃分子空间结构的研究中发现某一系列的烷烃分子只有一种一卤代物.如: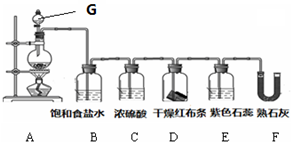 实验室用MnO2和浓盐酸制取氯气并验证氯气的部分性质,实验装置如图所示.
实验室用MnO2和浓盐酸制取氯气并验证氯气的部分性质,实验装置如图所示.