题目内容
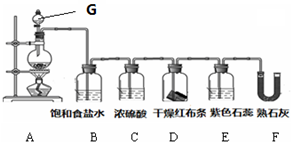 实验室用MnO2和浓盐酸制取氯气并验证氯气的部分性质,实验装置如图所示.
实验室用MnO2和浓盐酸制取氯气并验证氯气的部分性质,实验装置如图所示.(1)G装置名称
(2)B装置的作用是
(3)实验开始几分钟后,D装置红布条是否褪色,
(4)装置F中发生反应的化学方程式是
(5)F装置后应再连接一个尾气处理装置,装置里加入NaOH溶液,尾气处理的离子反应方程式为
考点:氯气的实验室制法
专题:实验题
分析:(1)根据装置G的构造写出其名称;根据氯气的实验室制法写出反应的离子方程式;反应中二氧化锰为氧化剂,氯化氢为氧化剂,参加反应的氯化氢中只有一半被氧化、做还原剂;
(2)氯化氢具有挥发性,制取的氯气中会混有氯化氢,B装置的作用就是出去氯气中的氯化氢;
(3)根据干燥的氯气不具有漂白性、湿润的氯气能够生成次氯酸,具有漂白性进行解答;根据氯水具有酸性、漂白性分析;
(4)氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水,据此写出反应的化学方程式;
(5)氢氧化钠溶液与氯气反应生成氯化钠、次氯酸钠和水,据此写出反应的离子方程式.
(2)氯化氢具有挥发性,制取的氯气中会混有氯化氢,B装置的作用就是出去氯气中的氯化氢;
(3)根据干燥的氯气不具有漂白性、湿润的氯气能够生成次氯酸,具有漂白性进行解答;根据氯水具有酸性、漂白性分析;
(4)氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水,据此写出反应的化学方程式;
(5)氢氧化钠溶液与氯气反应生成氯化钠、次氯酸钠和水,据此写出反应的离子方程式.
解答:
解:(1)A是氯气发生装置,二氧化锰和盐酸反应生成氯化锰、氯气和水,反应的离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
故答案为:分液漏斗; MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O; 1:2;
(2)氯气在饱和食盐水中溶解度较小,制取的氯气中会混有氯化氢,装置B中饱和食盐水的作用是除去氯气中混有的杂质氯化氢,
故答案为:除氯气中的氯化氢;
(3)干燥的氯气不会具有漂白性,所以D装置中干燥的红布条不褪色;氯气与水反应生成氯化氢和次氯酸,溶液显示酸性,所以紫色石蕊先变成红色,而次氯酸具有漂白性,所以很快红色会褪去,
故答案为:不褪色; 先变红后褪色;
(4)氯气与熟石灰反应的化学方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(5)氯气是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:Cl2+2OH-═Cl-+ClO-+H2O.
| ||
故答案为:分液漏斗; MnO2+4H++2Cl-
| ||
(2)氯气在饱和食盐水中溶解度较小,制取的氯气中会混有氯化氢,装置B中饱和食盐水的作用是除去氯气中混有的杂质氯化氢,
故答案为:除氯气中的氯化氢;
(3)干燥的氯气不会具有漂白性,所以D装置中干燥的红布条不褪色;氯气与水反应生成氯化氢和次氯酸,溶液显示酸性,所以紫色石蕊先变成红色,而次氯酸具有漂白性,所以很快红色会褪去,
故答案为:不褪色; 先变红后褪色;
(4)氯气与熟石灰反应的化学方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(5)氯气是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:Cl2+2OH-═Cl-+ClO-+H2O.
点评:本题考查了氯气的实验室制法、氯气的化学性质,题目难度中等,注意掌握氯气的实验室制法,明确氯气的化学性质是解答本题的关键,能够正确书写常见反应的离子方程式、化学方程式.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
对山林发生的重大火灾,下列方法适合的是( )
| A、砍掉或清理掉大火前面的干枯树枝、树叶等可燃物 |
| B、组织人力从山下运水到山上灭火 |
| C、用棉被等盖在大火上以隔绝空气 |
| D、打119火警电话,等待用水灭火 |
比较50ml 2mol/L HCl 溶液 和100ml 1mol/L MgCl2 溶液,它们( )
| A、所含Cl-的物质的量相等 |
| B、所含Cl-的浓度相等 |
| C、所含溶质的质量相等 |
| D、H+ 的浓度与Mg2+ 的浓度相等 |
 分子式:
分子式: