题目内容
 短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法正确的是( )
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法正确的是( )| A、Z位于元素周期表中第三周期ⅢA族 |
| B、原子半径的大小顺序为:X<Y |
| C、元素的最高价氧化物对应水化物的酸性R强于M |
| D、离子R-和Z3+的最外层电子数和电子层数都相同 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置,可知Z为Al、X为N元素、Y为O元素、M为S元素、R为Cl.
A.主族元素周期数等于电子层数、族序数=最外层电子数;
B.同周期自左而右原子半径减小;
C.非金属性越强,最高价含氧酸的酸性越强;
D.离子Cl-和Al3+的最外层电子数都是8,前者电子层为3、后者电子层为2.
A.主族元素周期数等于电子层数、族序数=最外层电子数;
B.同周期自左而右原子半径减小;
C.非金属性越强,最高价含氧酸的酸性越强;
D.离子Cl-和Al3+的最外层电子数都是8,前者电子层为3、后者电子层为2.
解答:
解:由元素在周期表中的位置,可知Z为Al、X为N元素、Y为O元素、M为S元素、R为Cl.
A.Z为Al元素,原子核外有3个电子层、最外层电子数为3,处于第三周期ⅢA族,故A正确;
B.同周期自左而右原子半径减小,故原子半径X>Y,故B错误;
C.同周期自左而右非金属性增强,故非金属性S<Cl,非金属性越强,最高价含氧酸的酸性越强,故高氯酸的酸性比硫酸强,故C正确;
D.离子Cl-和Al3+的最外层电子数都是8,前者电子层为3、后者电子层为2,二者电子层不相等,故D错误,
故选AC.
A.Z为Al元素,原子核外有3个电子层、最外层电子数为3,处于第三周期ⅢA族,故A正确;
B.同周期自左而右原子半径减小,故原子半径X>Y,故B错误;
C.同周期自左而右非金属性增强,故非金属性S<Cl,非金属性越强,最高价含氧酸的酸性越强,故高氯酸的酸性比硫酸强,故C正确;
D.离子Cl-和Al3+的最外层电子数都是8,前者电子层为3、后者电子层为2,二者电子层不相等,故D错误,
故选AC.
点评:本题考查元素周期表与元素周期律,难度中等,注意掌握原子半径比较、金属性与非金属性强弱比较.

练习册系列答案
相关题目
为了有效除去工业食盐中的Ca2+、Mg2+、SO42-,加入试剂的合理顺序为( )
| A、NaOH-Na2CO3-BaCl2 |
| B、NaOH-BaCl2-Na2CO3 |
| C、BaCl2-NaOH-Na2CO3 |
| D、Na2CO3-BaCl2-NaOH |
关于氨气的喷泉实验的说法不正确的是( )
| A、NH3用水做成喷泉实验,说明NH3易溶于水 |
| B、用标况下的NH3做成喷泉实验的烧瓶中的溶液的物质的量的浓度可以求出 |
| C、实验时,NH3越纯,效果越好 |
| D、若实验不成功,说明NH3不易溶于水 |
下列说法中,不正确的是( )
| A、在周期表里,所有元素所在的族序数等于原子核外最外层电子数 |
| B、在周期表里,所有元素所在周期序数等于原子核外电子层数 |
| C、族序数等于周期序数的主族元素性质与Al可能相似 |
| D、某一主族中非金属元素种类数等于族序数减2的绝对值 |
保护环境、爱护地球已成为人们的共同呼声.下列事实不会造成大气污染的是( )
| A、汽车尾气的大量排放 |
| B、化石燃料的大量使用 |
| C、火山爆发喷出的大量SO2 |
| D、水力发电 |
鉴定NaCl的最佳方法是( )
| A、焰色反应呈黄色,加硝酸酸化的AgNO3溶液有白色沉淀 |
| B、焰色反应呈紫色,加盐酸酸化的AgNO3溶液有白色沉淀 |
| C、焰色反应呈黄色,加盐酸酸化的AgNO3溶液有白色沉淀 |
| D、焰色反应呈紫色,加硝酸酸化的AgNO3溶液有白色沉淀 |
下列关于钠及其化合物叙述,正确的是( )
| A、硫酸钠灼烧时火焰呈紫色 |
| B、氧化钠可用于呼吸面具中作为氧气的来源 |
| C、碳酸钠的水溶液呈中性 |
| D、发酵粉中含有碳酸氢钠,能使焙制出的糕点疏松多孔 |
下列反应中不正确的是( )
A、用惰性电极电解AlCl3溶液:2Cl-+2H2O
| ||||
| B、明矾净水:Al3++3H2O?Al(OH)3+3H+ | ||||
| C、制备TiO2纳米粉:TiCl4+(x+2)H2O(过量)?TiO2?xH2O↓+4HCl | ||||
D、用铜为电极电解稀硫酸溶液:Cu+2H+
|
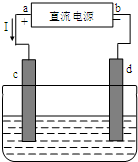 与图有关的下列叙述正确的是( )
与图有关的下列叙述正确的是( )| A、a为直流电源的负极 |
| B、用该装置制白铁(镀锌铁),d为铁电极 |
| C、用该装置精炼铜,d为粗铜电极 |
| D、c、d均为石墨电极电解饱和食盐水时,c电极附近pH升高 |