题目内容
18.在恒温时,一固定容积的容器内发生如下反应:3O2(g)?2O3(g)达平衡时,再向容器内通入一定量的O3(g),重新达到平衡后,与第一次平衡时相比,O3的体积分数( )| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法确定 |
分析 反应3O2(g)?2O3(g)达平衡后,再向容器内通入一定量的O3(g),可以等效为增大压强,平衡向正反应反应方向移动,据此进行解答.
解答 解:反应3O2(g)?2O3(g)达平衡后,再向容器内通入一定量的O3(g),可以等效为增大压强,平衡向正反应反应方向移动,重新达到平衡后,与第一次平衡时相比,O3的体积分数增大,
故选B.
点评 本题考查了化学平衡的影响,题目难度不大,明确化学平衡及其影响因素为解答关键,试题侧重考查学生的分析、理解能力及灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.某学生对SO2与漂粉精的反应进行实验探究:
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是碱性、漂白性.
(3)该同学推测现象1的白雾由HCl小液滴形成,并进行如下实验验证:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a的目的是检验白雾中是否含有Cl2,排除Cl2干扰.
②有同学认为由实验a、b不能判断白雾中含有HCl,理由是白雾中含有SO2,SO2可以使酸化的AgNO3溶液产生白色沉淀
(4)将A瓶中混合物过滤、洗涤,得到沉淀X.
①向沉淀X中加入稀HCl,无明显变化.取上层液体加氯化钡生成白色沉淀,则沉淀X是CaSO4
②用离子方程式解释现象4中黄绿色褪去的原因:Cl2+SO2+2H2O=4H++2Cl-+SO42-.
| 操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
 | 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀, 4.黄绿色褪去 |
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是碱性、漂白性.
(3)该同学推测现象1的白雾由HCl小液滴形成,并进行如下实验验证:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a的目的是检验白雾中是否含有Cl2,排除Cl2干扰.
②有同学认为由实验a、b不能判断白雾中含有HCl,理由是白雾中含有SO2,SO2可以使酸化的AgNO3溶液产生白色沉淀
(4)将A瓶中混合物过滤、洗涤,得到沉淀X.
①向沉淀X中加入稀HCl,无明显变化.取上层液体加氯化钡生成白色沉淀,则沉淀X是CaSO4
②用离子方程式解释现象4中黄绿色褪去的原因:Cl2+SO2+2H2O=4H++2Cl-+SO42-.
6.恒温下,向一个2L的密闭容器中充入1moN2和2.6molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
此条件下,该反应达到化学平衡时,氮气的浓度为0.4mol/L,平衡常数K=0.1.
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| C(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
13.硝基苯酚是合成医药、染料、感光材料的中间体;以苯酚为原料制备硝基苯酚的步骤如下:
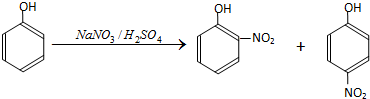
I.在常温下,向250mL三口烧瓶中加试剂(加入的试剂有:
A.50mL水;B.17.5gNaNO3;C.15mL浓硫酸
Ⅱ.称取4.7g苯酚,与1mL温水混合,并冷却至室温.
Ⅲ.在搅拌下,将苯酚水溶液自滴液漏斗滴入三口烧瓶中,将反应温度维持在20℃左右.
Ⅳ.加完苯酚后,继续搅拌1h,冷却至黑色油状物固化,倾出酸层.然后向油状物中加入20mL水并振摇,先倾出洗液,再用水洗三次,以除净残存的酸..
V.邻硝基苯酚的提纯.固化的黑色油状物主要成分是邻硝基苯酚和对硝基苯酚.
(1)步骤I中加入试剂的先后顺序为ACB(填序号)
(2)苯酚有腐蚀性,步骤Ⅱ中若不慎使苯酚触及皮肤,应立刻用酒精棉擦洗.苯酚中加少许水可降低熔点,使其中室温下即呈液态,这样操作的作用是便于滴加,同时也可以加快反应.
(3)步骤Ⅲ中,将反应温度维持在20℃左右的原因是当温度过高,一元硝基酚有可能发生进步硝化,当温度偏低,又将减缓反应速度.
(4)步骤Ⅳ中,若黑色油状物未固化,则可用分液漏斗(填实验仪器)将黑色油状物分出.
(5)根据题给信息,不使用温度计,设计步骤V得到纯净的邻硝基苯酚的实验方案;对油状混合物作水蒸气蒸馏,将馏出液冷却过滤,收集晶体,即得邻硝基苯酚产物.

I.在常温下,向250mL三口烧瓶中加试剂(加入的试剂有:
A.50mL水;B.17.5gNaNO3;C.15mL浓硫酸
Ⅱ.称取4.7g苯酚,与1mL温水混合,并冷却至室温.
Ⅲ.在搅拌下,将苯酚水溶液自滴液漏斗滴入三口烧瓶中,将反应温度维持在20℃左右.
Ⅳ.加完苯酚后,继续搅拌1h,冷却至黑色油状物固化,倾出酸层.然后向油状物中加入20mL水并振摇,先倾出洗液,再用水洗三次,以除净残存的酸..
V.邻硝基苯酚的提纯.固化的黑色油状物主要成分是邻硝基苯酚和对硝基苯酚.
| 密度 (g•mL-1) | 熔点 (℃) | 沸点 (℃) | 溶解性 | 其他 | |
| 邻硝基苯酚 | 1.495 | 44.45 | 214 | 微溶于冷水,易溶于热水 | 能与水蒸气一同挥发 |
| 对硝基苯酚 | 11.481 | 113.4 | 279 | 稍溶于水 | 不与水蒸气一同挥发 |
(2)苯酚有腐蚀性,步骤Ⅱ中若不慎使苯酚触及皮肤,应立刻用酒精棉擦洗.苯酚中加少许水可降低熔点,使其中室温下即呈液态,这样操作的作用是便于滴加,同时也可以加快反应.
(3)步骤Ⅲ中,将反应温度维持在20℃左右的原因是当温度过高,一元硝基酚有可能发生进步硝化,当温度偏低,又将减缓反应速度.
(4)步骤Ⅳ中,若黑色油状物未固化,则可用分液漏斗(填实验仪器)将黑色油状物分出.
(5)根据题给信息,不使用温度计,设计步骤V得到纯净的邻硝基苯酚的实验方案;对油状混合物作水蒸气蒸馏,将馏出液冷却过滤,收集晶体,即得邻硝基苯酚产物.
7.除去括号内杂质所用试剂和方法不正确的是( )
| A. | Cu(Fe)----加盐酸,过滤 | B. | NaCl溶液(碘)----CCl4,萃取、分液 | ||
| C. | KCl溶液(KNO3)----降温结晶,过滤 | D. | Cl2(HCl)----饱和氯化钠溶液,洗气 |