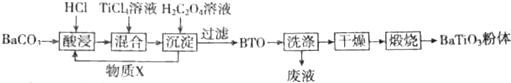
��Ŀ����
7������������SnSO4����һ����Ҫ�������Σ���Ҫ���ڵ�ƹ�ҵ�Ķ��������Ͻ�����������ɫ��ӡȾ��ҵ��ýȾ����˫��ˮȥ�����ȣ�ij�о�С�����SnSO4�Ʊ�·�����£�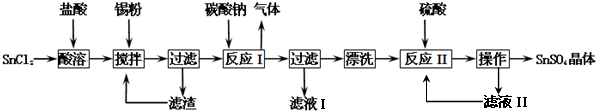
�������ϣ�
�����������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ�������
��SnCl2��ˮ������������Sn��OH��Cl����ʽ�Ȼ���������
��Sn��OH��2��������Al��OH��3�������ƣ���ش��������⣺
��1��SnCl2��ĩ���Ũ��������ܽ⣬����������ԭ���Ǽ������ᣬʹˮ��ƽ�������ƶ�������Sn2+ˮ�⣮
��2����Ӧ��õ�������SnO���õ��ó��������ӷ���ʽ��Sn2++CO32-�TSnO��+CO2����
��3����Һ�����ʵijɷ���NaCl��Na2CO3��
��4�����������£�SnSO4����������˫��ˮȥ������������Ӧ�����ӷ���ʽ��Sn2++H2O2+2H+=Sn4++2H2O��
��5����ȡSnSO4•x H2O����50.2g���ڸ��������������С��������ᾧˮȫ��ʧȥ����ȴ������������Ϊ43g����ʽ����þ���Ļ�ѧʽΪSnSO4•2H2O��
���� SnCl2��ĩ��Ũ��������ܽ�õ�������Һ����ʱ��Һ�к���Sn2+��Sn4+�������м���Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpHֵ������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+�����˵�SnCl2��Һ�������м�̼���ƣ���SnԪ����SnO��ʽ����������ϴ�ӵô�����SnO����ӦI��Һ������Ϊ�Ȼ��ƺ�̼���ƣ�SnO�м�ϡ���ᣬ��SnSO4��Һ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ��Ƶ�SnSO4���壬
��1��SnCl2��ˮ�з���ˮ�ⷴӦ������HCl����ʹˮ��ƽ�����淴Ӧ�����ƶ�������Sn2+ˮ�⣻
��2����Ӧ��Ϊ��SnCl2��Һ�м�̼���ƣ��õ��ij���ΪSnO�����ݵ���غ��Ԫ���غ���д���ӷ���ʽ��
��3����ӦI��Һ������Ϊ�Ȼ��ƺ�̼���ƣ�����ͨ�������ᾧ�ķ���������ʣ�
��4�����������£�SnSO4����������˫��ˮȥ��������SnSO4�����������º�˫��ˮ��Ӧ��Sn2+�л�ԭ�ԣ�˫��ˮ�������ԣ�����Ӧ���ǣ�Sn4+��H2O��
��5�����ݷ�ӦSnSO4•x H2O$\frac{\underline{\;\;��\;\;}}{\;}$SnSO4+x H2O���ɾ��弰���ɹ���������б���ʽ�����x��ֵ��
��� �⣺SnCl2��ĩ��Ũ��������ܽ�õ�������Һ����ʱ��Һ�к���Sn2+��Sn4+�������м���Sn�ۣ�Sn�ۿ��Ժ�H+������Ӧ��ʹ��Һ���Լ�������������ҺpHֵ������Sn���Խ����������ɵ�Sn4+��ԭ��Sn2+������ֹSn2+������ΪSn4+�����˵�SnCl2��Һ�������м�̼���ƣ���SnԪ����SnO��ʽ����������ϴ�ӵô�����SnO����ӦI��Һ������Ϊ�Ȼ��ƺ�̼���ƣ�SnO�м�ϡ���ᣬ��SnSO4��Һ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ��Ƶ�SnSO4���壬
��1��SnCl2��ˮ�з���ˮ�ⷴӦ��SnCl2+H2O�TSn��OH��Cl+HCl�����淴Ӧ��Ӧ���ÿ���ţ�������������Sn��OH��Cl����Һ�������ʣ�������HCl����ʹƽ�����淴Ӧ�����ƶ�������Sn2+ˮ�⣻
�ʴ�Ϊ���������ᣬʹˮ��ƽ�������ƶ�������Sn2+ˮ�⣻
��2����Ӧ��Ϊ��SnCl2��Һ�м�̼���ƣ��õ��ij���ΪSnO����Ӧ���ӷ���ʽΪSn2++CO32-�TSnO��+CO2����
�ʴ�Ϊ��Sn2++CO32-�TSnO��+CO2����
��3����ӦI��Һ������Ϊ�Ȼ��ƺ�̼���ƣ�����ͨ�������ᾧ�ķ����������ΪNaCl��Na2CO3��
�ʴ�Ϊ��NaCl��Na2CO3��
��4�����������£�SnSO4����������˫��ˮȥ��������SnSO4�����������º�˫��ˮ��Ӧ��Sn2+�л�ԭ�ԣ�˫��ˮ�������ԣ�����Ӧ���ǣ�Sn4+��H2O������ʽΪSn2++H2O2+2H+=Sn4++2H2O��
�ʴ�Ϊ��Sn2++H2O2+2H+=Sn4++2H2O��
��5�����ݷ�ӦSnSO4•x H2O$\frac{\underline{\;\;��\;\;}}{\;}$SnSO4+x H2O��
215+18x 215
50.2g 43g
��$\frac{215+18x}{50.2}$=$\frac{215}{43}$��x=2�����Ըþ���Ļ�ѧʽΪ��SnSO4•2H2O��
�ʴ�Ϊ��SnSO4•2H2O��
���� ���⿼�������ʷ���ķ�����ʵ������������ζ�ʵ��ļ����жϺͼ���Ӧ�ã���Ŀ�Ѷ��еȣ���ȷʵ��Ŀ�ļ�ʵ��ԭ��Ϊ���ؼ�������������ѧ���ķ�����������������ѧʵ��������

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ��״���£�1molNa2O2��22.4LCO2��Ӧ��ת�Ƶ�����Ϊ1mol | |
| B�� | ����Ͷ�뵽CuSO4��Һ�У������û�����Cu | |
| C�� | ��Na2O2Ͷ�뵽FeSO4��Һ�У������ɺ��ɫ���� | |
| D�� | ������ͭ��ϡ�����Ӧ������KNO3������������� |

| A�� | ȡ����Ӧ | B�� | �ӳɷ�Ӧ | C�� | ˮ�ⷴӦ | D�� | �Ӿ۷�Ӧ |
��1����֪N2��g��+O2��g��=2NO��g����H=+180.5KJ•mol-1
2CO��g��+O2��g��=2CO2��g����H=-566.0KJ•mol-1
��Ӵ�����������β�����Ȼ�ѧ������2CO��g��+2NO��g��=2CO2��g��+N2��g����H=-746.5KJ•mol-1
��2����Ӧ2NO2��g��?2NO��g��+O2��g�� ���ݻ�Ϊ2.0L���ܱ������н��У���Ӧ������NO2�����ʵ�����ʱ��ı仯���
| ʱ�䣨s�� | 0 | 10 | 20 | 25 | 30 |
| ����A[n��NO2��]��mol�� | 0.20 | 0.14 | 0.13 | 0.13 | 0.13 |
| ����B[n��NO2��]��mol�� | 0.20 | 0.10 | 0.10 | 0.10 | 0.10 |
A���С����� B���¶Ȳ�ͬ C��ѹǿ��ͬ D�����������ͬ
����˵���÷�Ӧ�Ѵﵽƽ��״̬����ACE
A��V����NO2��=V�棨NO�� B��c��NO2��=c��NO�� C��O2�����ʵ�������
D�����������ܶȲ��� E����������ƽ��Ħ������
��������A�ӷ�Ӧ��ʼ��10sʱ��������ƽ������Ϊ0.0015mol•L-1•s-1
��������B���䱣��ѹǿ����������£���ƽ����ϵ����ͨ��0.15molO2��0.1molNO2����Ӧ����������������ƶ�������
| ѡ�� | ��ѧ��Ӧ�� ���ӷ���ʽ | �� �� |
| A | ����������ˮ��CH3COO-+H2O�TCH3COOH+OH- | ��ȷ |
| B | ʵ������Ũ������MnO2��Ӧ��Cl2�� MnO2+4H++2Cl- $\frac{\underline{\;\;��\;\;}}{\;}$Cl2��+Mn2++2H2O | ����Ӧ����HCl�������H+��Cl-����Ϊ1��1 |
| C | ��������Һ�мӹ�����ˮ��Fe3++3NH3•H2O�TFe��OH��3�����壩+3NH4+ | ����Fe��OH��3Ӧ���dz��� |
| D | ������̼���У�2Al+3H2CO3�T2Al3++3H2+3 CO32- | ��ȷ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ����Ӧ��Ũ�ȣ����������Ӱٷ������Ӷ�ʹ��Ч��ײ�������� | |
| B�� | ������μӵĻ�ѧ��Ӧ��������ѹǿ������С��Ӧ����������������������ӵİٷ������Ӷ�ʹ��Ӧ�������� | |
| C�� | �����¶���ʹ��Ӧ����������Ҫԭ���������˷�Ӧ�����Ũ�� | |
| D�� | ʹ�����������������Ӱٷ������Ӷ�����������ѧ��Ӧ���� |