题目内容
3.下列叙述中,错误的是( )| A. | 虽然固体氯化钠不能导电,但氯化钠是电解质 | |
| B. | 在纯水中加入少量硫酸铵,可抑制水的电离 | |
| C. | 在醋酸钠溶液中加入少量氢氧化钠,溶液中 c(OH-)增大 | |
| D. | 纯水的pH随温度的升高而减小 |
分析 A.溶于水或者熔融状态下能导电的化合物为电解质;
B.依据水的电离平衡移动影响因素解答;
C.氢氧化钠为强碱,完全电离;
D.依据水的电离为吸热过程判断温度对水PH影响.
解答 解:A.虽然固体氯化钠不能导电,但是氯化钠溶于水或者熔融状态下都能导电,所以是电解质,故A正确;
B在纯水中加入少量硫酸铵,铵根离子水解,促进水的电离,故B错误;
C.在醋酸钠溶液中加入少量氢氧化钠,尽管抑制醋酸根离子的水解,但氢氧化钠为强碱,完全电离,所以溶液中c(OH-)仍增大,故C正确;
D.水的电离为吸热过程,升高温度促进水的电离,氢离子浓度增大,所以溶液pH减小,故D正确;
故选:B.
点评 本题考查了电解质的判断,影响电解质电离平衡的因素,明确电解质概念及弱电解质电离平衡移动的影响因素是解题关键,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
4.下列的描述中不正确的是( )
| A. | 常温下,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1mol | |
| B. | 一定条件下的可逆反应,反应物的转化率不可能达到100% | |
| C. | 沉淀溶解转换的实质是沉淀溶解平衡的移动,平衡一般向生成更难溶物质的方向移动 | |
| D. | △H<0,△S>0的反应一定是自发进行的化学反应 |
11.要将溴水中的溴提取出来,需要用到的一组仪器是( )
| A. | 普通漏斗、玻璃棒、烧杯 | B. | 长颈漏斗、玻璃棒、烧杯 | ||
| C. | 大试管、试管夹、容量瓶 | D. | 分液漏斗、烧杯、铁架台 |
8.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A. | 离子半径大小顺序:r(Z2+)>r(Y2-) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应水化物的酸性比W的弱 | |
| D. | Y的气态简单氢化物的热稳定性比W的强 |
15.根据不同部位工作条件的不同,航天飞机使用了多种防热材料.例如,机身和机翼下表面使用高温陶瓷瓦.下列对新型陶瓷材料的有关叙述中,错误的是( )
| A. | 高温结构陶瓷属于新型无机非金属材料,可以作为高级耐火材料 | |
| B. | 氧化铝陶瓷属于新型无机非金属材料,它是生物陶瓷 | |
| C. | 氮化硅陶瓷属于新型无机非金属材料,可用于制造陶瓷发动机的受热面 | |
| D. | 新型无机非金属材料克服了传统无机非金属材料的缺点,但是强度比较差 |
12.已知:H2(g)+F2(g)→2HF(g)+270KJ,下列说法正确的是( )
| A. | 2L氟化氢气体分解成1L氟气与1L氢气吸收270KJ热量 | |
| B. | 1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270KJ | |
| C. | 在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量 | |
| D. | 一个氢气分子与一个氟气分子反应生成2个氟化氢气体分子放出270KJ热量 |
13.已知反应4CO+2NO2?N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
| A. | v(CO)=0.025 mol•L-1•S-1 | B. | v(NO2)=0.7 mol•L-1•min-1 | ||
| C. | v(N2)=0.36 mol•L-1•min-1 | D. | v(CO2)=1.1 mol•L-1•min-1 |
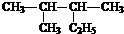 2,3-二甲基戊烷;
2,3-二甲基戊烷;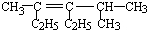 3,5-二甲基-4-乙基-3-己烯.
3,5-二甲基-4-乙基-3-己烯.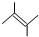 .
.