题目内容
实验证明:不同浓度的HNO3与同一金属反应可生成不同的还原产物.例如,镁与硝酸反应实验中,测得其气体产物有H2、N2、NO、NO2,溶液中产物有Mg(NO3)2,NH4NO3和H2O.生成这些产物的HNO3浓度范围见下表.
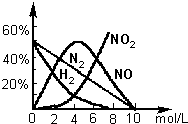
各气体产物成分及含量随HNO3浓度变化曲线如图所示.

(1)若硝酸与镁反应只生成N2气体,则反应的化学方程式为:________.
(2)1.2 g Mg与足量4 mol/L的HNO3完全反应,收集到280 mL(S.T.P)混合气体,其体积分别为H2________mL、N2________mL、NO________mL、NO2________mL.除了上述混合气体外,是否还有其它还原产物?答:________.
答案:
解析:
解析:
|
(1)5Mg+12HNO3=5Mg(NO3)2+N2↑+6H2O(3分) (2)28 84 140 28 有(每空1分) |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 HNO3是极其重要的化工原料.工业上制备HNO3采用NH3催化氧化法,将中间产生的NO2在密闭容器中多次循环用水吸收制备的.
HNO3是极其重要的化工原料.工业上制备HNO3采用NH3催化氧化法,将中间产生的NO2在密闭容器中多次循环用水吸收制备的.