题目内容
如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)![]() xC(g);ΔH<0
xC(g);ΔH<0
平衡时A、B、C的物质的量之比为1:3:4,C的物质的量为y mol.
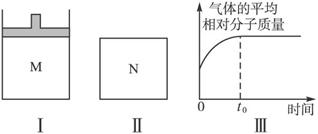
(1)根据题中数据计算,x=____________、y=___________.
(2)如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其他条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol.由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①,可不填满):
可能的情形 | A、B是否为气态 | z与y的大小关系 | M(B)与M(C) 的大小关系(M表示摩尔质量) | |
A | B | |||
① | 是 | 不是 | z=y | 无法确定 |
② |
|
|
|
|
③ |
|
|
|
|
(1)2 1.6
(2)
|
|
|
| |
|
| |||
|
|
|
|
|
| 是 | 是 | z<y | 无法确定 |
| 不是 | 是 | z<y | M(B)<M(C) |
解析:(1)设达平衡时B反应的物质的量为a,则:
2A + B ![]() xC
xC
起始量:2 2 0
转化量:2a a ax
平衡量:2-2a 2-a ax
由(2-2a):(2-a):ax=1:3:4可得a=0.8 mol,x=2,y=ax=1.6 mol.
(2)②若A、B均为气态,则M相当于N达平衡时再加压,所以y>z,M(B)、M(C)大小无法确定.
③若A为非气态,B为气态,则正向为体积增大的反应,所以M相当于N达平衡时再减压,所以y>z,起始态只有B为气态,M(气体)=M(B),平衡时为B、C混合气,而M(混合物)>M(B),所以M(C)>M(B).

如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2 A(?)+B(?) x C(g);ΔH<0
x C(g);ΔH<0
平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。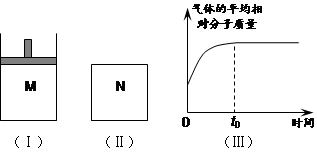
⑴根据题中数据计算,x =_________、y =_________;
⑵如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
| 可能的情形 | A、B是否为气态 | z与y的大小关系 | M(B)与M(C)的大小关系 (M表示摩尔质量) | |
| A | B | |||
| ① | 是 | 不是 | z =y | 不确定 |
| ② | | | | |
| ③ | | | | |
(10分)如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:
2 A(?)+B(?) x C(g);ΔH<0
x C(g);ΔH<0
平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。
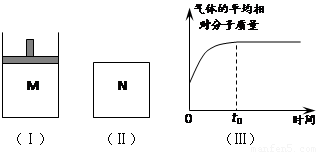
⑴根据题中数据计算,x =_________、y =_________;
⑵如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
|
可能的情形 |
A、B是否为气态 |
z与y的大小关系 |
M(B)与M(C)的大小关系 (M表示摩尔质量) |
|
|
A |
B |
|||
|
① |
是 |
不是 |
z = y |
前面的结论与此无关 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
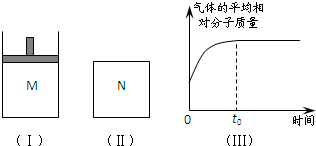 (2008?湖南模拟)如图Ⅰ,在恒压密闭容器M中加入2mol A和2mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?x C(g);△H<0
(2008?湖南模拟)如图Ⅰ,在恒压密闭容器M中加入2mol A和2mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?x C(g);△H<0
 xC(g) ΔH<0平衡时M中A、B、C的物质的量之比为 1∶3∶2。下列判断正确的是
xC(g) ΔH<0平衡时M中A、B、C的物质的量之比为 1∶3∶2。下列判断正确的是