题目内容
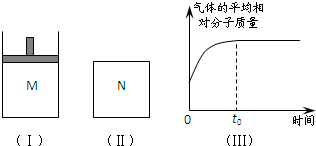 (2008?湖南模拟)如图Ⅰ,在恒压密闭容器M中加入2mol A和2mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?x C(g);△H<0
(2008?湖南模拟)如图Ⅰ,在恒压密闭容器M中加入2mol A和2mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?x C(g);△H<0平衡时A、B、C的物质的量之比为1:3:4,C的物质的量为 y mol.
(1)根据题中数据计算,x=
2
2
、y=1.6
1.6
;(2)如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol.由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
| 可能的情形 | A、B是否为气态 | z与y的大小关系 | M(B)与M(C)的大小关系 (M表示摩尔质量) | |
| A | B | |||
| ① | 是 | 不是 | z=y | 无法确定 |
| ② | 是 是 |
是 是 |
y>z y>z |
无法确定 无法确定 |
| ③ | 不是 不是 |
是 是 |
y>z y>z |
M(C)>M(B) M(C)>M(B) |
分析:设达平衡时B反应的物质的量为n mol,则:2A(?)+B(?)?x C(g)
起始量(mol):2 2 0
转化量(mol):2n n nx
平衡量(mol):2-2n 2-n nx
由(2-2n):(2-n):nx=1:3:4,解得n=0.8 mol,x=2,
②若A、B均为气态,则M相当于N达平衡时再加压,M(B)、M(C)大小无法确定;
③若A为非气态,B为气态,则正向为体积增大的反应,所以M相当于N达平衡时再减压,起始态只有B为气态,M(气体)=M(B),平衡时为B、C混合气,由图可知M(混合物)>M(B),据此确定M(B)、M(C)大.
起始量(mol):2 2 0
转化量(mol):2n n nx
平衡量(mol):2-2n 2-n nx
由(2-2n):(2-n):nx=1:3:4,解得n=0.8 mol,x=2,
②若A、B均为气态,则M相当于N达平衡时再加压,M(B)、M(C)大小无法确定;
③若A为非气态,B为气态,则正向为体积增大的反应,所以M相当于N达平衡时再减压,起始态只有B为气态,M(气体)=M(B),平衡时为B、C混合气,由图可知M(混合物)>M(B),据此确定M(B)、M(C)大.
解答:解:(1)设达平衡时B反应的物质的量为n mol,则:2A(?)+B(?)?x C(g)
起始量(mol):2 2 0
转化量(mol):2n n nx
平衡量(mol):2-2n 2-n nx
由(2-2n):(2-n):nx=1:3:4,解得n=0.8 mol,x=2,则y=nx=1.6,
故答案为:2;1.6;
(2)②若A、B均为气态,则M相当于N达平衡时再加压,N的平衡向右移动,所以y>z,M(B)、M(C)大小无法确定;
③若A为非气态,B为气态,则正向为体积增大的反应,所以M相当于N达平衡时再减压,N的平衡向右移动,所以y>z,起始态只有B为气态,M(气体)=M(B),平衡时为B、C混合气,而M(混合物)>M(B),所以M(C)>M(B),
故答案为:
.
起始量(mol):2 2 0
转化量(mol):2n n nx
平衡量(mol):2-2n 2-n nx
由(2-2n):(2-n):nx=1:3:4,解得n=0.8 mol,x=2,则y=nx=1.6,
故答案为:2;1.6;
(2)②若A、B均为气态,则M相当于N达平衡时再加压,N的平衡向右移动,所以y>z,M(B)、M(C)大小无法确定;
③若A为非气态,B为气态,则正向为体积增大的反应,所以M相当于N达平衡时再减压,N的平衡向右移动,所以y>z,起始态只有B为气态,M(气体)=M(B),平衡时为B、C混合气,而M(混合物)>M(B),所以M(C)>M(B),
故答案为:
| A、B是否为气态 | z与y的大小关系 | M(B)与M(C)的大小关系 (M表示摩尔质量) | ||
| ② | 是 | 是 | y>z | 无法确定 |
| ③ | 不是 | 是 | y>z | M(C)>M(B) |
点评:本题考查化学平衡计算,难度中等,(2)中关键是利用等效思想构建平衡建立的途径便于比较,注意利用平衡时与起始时相对分子质量大小判断B、C的相对分子质量关系.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目