题目内容
(2013?芜湖模拟)混合下列各组物质,加热蒸干并在300℃灼烧至质量不变,最终残留固体为纯净物的是( )
分析:A、加热时氯化铝会水解生成氢氧化铝,蒸干溶液继续灼烧,则氢氧化铝分解生成氧化铝,硫酸铝蒸干并灼烧后还是硫酸铝;
B、等物质的量浓度、等体积的(NH4)2SO4溶液与BaCl2溶液混合恰好生成硫酸钡和氯化铵;
C、发生的反应为:
Na2O2 +H2O=2NaOH+
O2
NaHCO3 +NaOH=Na2CO3+H2O
由于Na2O2与NaHCO3等物质的量,所以NaOH是NaHCO3量的二倍,所以NaOH过量;
D、Na2SO3 +Cl2+2NaOH=Na2SO4 +2NaCl+H2O.
B、等物质的量浓度、等体积的(NH4)2SO4溶液与BaCl2溶液混合恰好生成硫酸钡和氯化铵;
C、发生的反应为:
Na2O2 +H2O=2NaOH+
| 1 |
| 2 |
NaHCO3 +NaOH=Na2CO3+H2O
由于Na2O2与NaHCO3等物质的量,所以NaOH是NaHCO3量的二倍,所以NaOH过量;
D、Na2SO3 +Cl2+2NaOH=Na2SO4 +2NaCl+H2O.
解答:解:A、加热时氯化铝会水解(生成的HCl受热从溶液中逸出,促进水解进行)生成氢氧化铝,蒸干溶液继续灼烧,则氢氧化铝分解生成氧化铝,硫酸铝蒸干并灼烧后还是硫酸铝,故等物质的量的硫酸铝与氯化铝加热蒸干并在300℃灼烧至质量不变,最终残留固体为氧化铝和硫酸铝的混合物,故A错误;
B、等物质的量浓度、等体积的(NH4)2SO4溶液与BaCl2溶液混合恰好生成硫酸钡和氯化铵,氯化铵加热分解,加热蒸干、灼烧,氯化铵分解,残留固体为硫酸钡,故B正确;
C、发生的反应为:
Na2O2 +H2O=2NaOH+
O2
NaHCO3 +NaOH=Na2CO3+H2O
由于Na2O2与NaHCO3等物质的量,所以NaOH是NaHCO3量的二倍,所以NaOH过量,因此残留固体是碳酸钠和氢氧化钠的混合物,故C错误;
D、Na2SO3 +Cl2+2NaOH=Na2SO4 +2NaCl+H2O,因此残留固体是硫酸钠和氯化钠的混合物,故D错误,
故选B.
B、等物质的量浓度、等体积的(NH4)2SO4溶液与BaCl2溶液混合恰好生成硫酸钡和氯化铵,氯化铵加热分解,加热蒸干、灼烧,氯化铵分解,残留固体为硫酸钡,故B正确;
C、发生的反应为:
Na2O2 +H2O=2NaOH+
| 1 |
| 2 |
NaHCO3 +NaOH=Na2CO3+H2O
由于Na2O2与NaHCO3等物质的量,所以NaOH是NaHCO3量的二倍,所以NaOH过量,因此残留固体是碳酸钠和氢氧化钠的混合物,故C错误;
D、Na2SO3 +Cl2+2NaOH=Na2SO4 +2NaCl+H2O,因此残留固体是硫酸钠和氯化钠的混合物,故D错误,
故选B.
点评:考查物质之间的反应及物质性质,涉及过量问题,难度中等,注意水解和分解.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
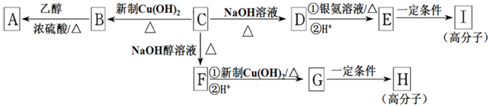



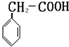 或
或 或
或 或
或
