题目内容
实验室制完氯气后,用下列哪一种溶液吸收残余氯气( )
| A、NaOH溶液 | B、Na2CO3溶液 | C、浓H2SO4 | D、NaCl溶液 |
分析:氯气有毒,不能排放在环境中,应利用碱液吸收尾气,以此来解答.
解答:解:A.氯气与NaOH反应生成NaCl、NaClO、水,且吸收效果好,故A正确;
B.碳酸钠溶液的碱性太弱,虽能与氯气反应,但吸收效果不好,故B错误;
C.氯气与浓硫酸不反应,不能吸收氯气,故C错误;
D.NaCl溶液抑制氯气的溶解,不能吸收氯气,故D错误;
故选A.
B.碳酸钠溶液的碱性太弱,虽能与氯气反应,但吸收效果不好,故B错误;
C.氯气与浓硫酸不反应,不能吸收氯气,故C错误;
D.NaCl溶液抑制氯气的溶解,不能吸收氯气,故D错误;
故选A.
点评:本题考查氯气的化学性质,为高频考点,把握氯气与碱的反应及尾气处理的要求为解答的关键,注意有毒气体不能排放在环境中,应充分吸收尾气,侧重基础知识的考查,题目难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种.
(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为: .
(2)实验室用二氧化锰制取氯气的化学方程式为: ;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号).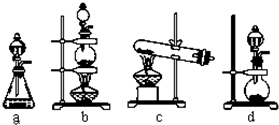
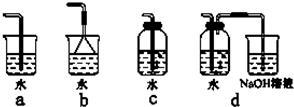
(3)实验室中模拟Br-→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现.写出Br-→Br2的转化离子方程式为: ;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是 (选填下列选项的编号字母).
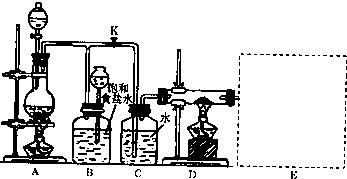
(4)实验室制备氯气的反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如下图),再把已称好50.0g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应.观察读数变化如下表所示:

请你据此分析计算:
①实验中产生的CO2气体质量为 ;
②残余液中盐酸的物质的量浓度为(结果精确到小数点后一位) .
(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为:
(2)实验室用二氧化锰制取氯气的化学方程式为:

(3)实验室中模拟Br-→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现.写出Br-→Br2的转化离子方程式为:

(4)实验室制备氯气的反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如下图),再把已称好50.0g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应.观察读数变化如下表所示:

| CaCO3用量 | 未加CaCO3时 | 加约四分之一时 | 加一半时 | 全部加完时 |
| 读数/g | 318.3 | 325.3 | 334.5 | 359.5 |
①实验中产生的CO2气体质量为
②残余液中盐酸的物质的量浓度为(结果精确到小数点后一位)
 (1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有
(1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有
 (1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有______.
(1)①要配制500mL 0.200mol?L-1的H2SO4溶液,需要的仪器除量筒、烧杯外还有______.