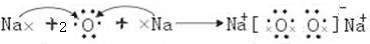题目内容
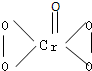
在过氧化物中加入乙醚后,再加入数滴K2Cr2O7的硫酸溶液,轻轻振荡后静置,乙醚层呈现蓝色,这是由于生成的过氧化铬(CrO5)溶于乙醚之故。CrO5的结构式如图所示 。
。
(1)在CrO5中氧元素的化合价为________。
(2)写出这一反应的离子方程式__________________________。
(3)这个反应______(填“是”或“不是”)氧化还原反应,其理由是________。
(1)1个氧原子显-2价,4个氧原子显-1价。
(2)Cr2O72- +4H2O2+2H+ = 2CrO5+5H2O
(3)不是。该反应中反应前后元素的化合价没有发生变化。
(观察过氧化铬的结构式或知,其中铬元素的化合价是+5价,重铬酸钾转化为过氧化铬属于非氧化还原反应)

练习册系列答案
相关题目
I.在过氧化氢中加入乙醚后,再加入数滴K2Cr2O7的硫酸溶液,轻轻振荡后静置,乙醚层呈蓝色,这是由于生成的过氧化铬(CrO5)溶于乙醚的缘故.已知过氧化铬的结构简式为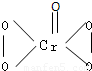 ?
?
(1)CrO5中氧元素的化合价为 .
(2)上述反应的离子方程式为 .
Ⅱ.下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.
(1)i元素名称是 .
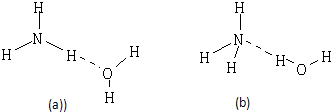
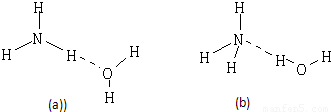
(2)NH3?H2O的电离方程式为NH3?H2O?NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是 .(填序号)
(3)用电子式表示e的过氧化物的形成过程 .
(4)利用稀有气体化合物,人们实现了许多制备实验上的突破.如XeO3在一定条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式: .
 ?
?(1)CrO5中氧元素的化合价为 .
(2)上述反应的离子方程式为 .
Ⅱ.下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j | ||||||||||||||||
(2)NH3?H2O的电离方程式为NH3?H2O?NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是 .(填序号)

(3)用电子式表示e的过氧化物的形成过程 .
(4)利用稀有气体化合物,人们实现了许多制备实验上的突破.如XeO3在一定条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式: .


 ?
?