题目内容
1.NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 过氧化钠与水反应时,生成0.1molO2转移的电子数为0.2NA | |
| B. | 4.48L氨气分子中含0.6NA个N-H键 | |
| C. | 100ml0.2mol•L-1的FeCl3溶液中,含Fe3+数为0.02NA | |
| D. | 密闭容器中2molNO与1molO2充分反映,产物的分子数为2NA |
分析 A、过氧化钠和水反应时,氧元素由-1价变为0价;
B、氨气所处的状态不明确;
C、铁离子为弱碱阳离子,在溶液中会水解;
D、NO和氧气反应后生成的NO2中存在平衡:2NO2?N2O4.
解答 解:A、过氧化钠和水反应时,氧元素由-1价变为0价,故当生成0.1mol氧气时转移0.2NA个电子,故A正确;
B、氨气所处的状态不明确,故其物质的量无法计算,故B错误;
C、铁离子为弱碱阳离子,在溶液中会水解,故溶液中的铁离子的个数小于0.02NA个,故C错误;
D、NO和氧气反应后生成的NO2中存在平衡:2NO2?N2O4,导致分子个数减少,故产物分子个数小于2NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
11.将Zn和Cu用导线连接置于同一稀H2SO4溶液中,下列各叙述中正确的是( )
| A. | 正极附近C(H+)逐渐增大 | |
| B. | 正极上产生气泡 | |
| C. | 正极、负极附近C(H+)基本不变 | |
| D. | Zn片、Cu片同时冒出气泡,则说明Zn片不纯 |
12.在pH=1的某无色透明溶液中,能大量共存的离子组是( )
| A. | NH4+、K+、SO42-、Br- | B. | K+、Na+、AlO2-、Cl- | ||
| C. | Fe3+、K+、SO42-、NO3- | D. | K+、Na+、NO3-、I- |
9.下列离子方程式不正确的是( )
| A. | 硫化亚铁和稀盐酸反应:FeS+2H+=Fe2++H2S↑ | |
| B. | 次氯酸钠溶液中通入少量SO2反应:SO2+H2O+ClO-=SO42-+Cl-+2H+ | |
| C. | 过氧化钠加入足量稀硫酸反应:2Na2O2+4H+═4Na++O2↑+2H2O | |
| D. | 铜粉中加入溴化铁溶液反应:2Fe3++Cu=2Fe2++Cu2+ |
6.化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )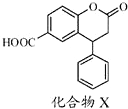

| A. | 分子式为C16H14O4 | |
| B. | 1mol化合物X在一定条件下最多加成6molH2 | |
| C. | 分子中有三种官能团,酸性条件下水解后官能团还是三种 | |
| D. | 1mol化合物X最多能与2molNaOH反应 |
13.下列有关实验操作正确且能达到实验目的或得出相应结论的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 用激光笔分别照射蛋白质溶液、硅酸溶胶 | 将二者区别开 |
| B | 将C2H5OH与浓H2SO4在蒸馏烧瓶中混合后加热至 170℃,烧瓶内逸出的物质通入到酸性KMnO4溶液中 | 检验有无乙烯生成 |
| C | 将Al(OH)3置于适量0.2mol•L-1 FeCl3溶液中,-段时间后可得到红褐色固体 | 溶度积:Ksp[AL(OH)3]>Ksp[Fe(OH)3] |
| D | 向蔗糖溶液中加入适量稀硫酸,水浴加热几分钟,然后加入新制的银氨溶液,并水浴加热 | 检验蔗糖的水解产物是否具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
10.推理是化学学习中常用的思维方法.下列推理中正确的是( )
| A. | 单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质 | |
| B. | 氧元素与硫元素原子的最外层电子数相同,所以二者具有相似的化学性质 | |
| C. | 溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小 | |
| D. | 碱溶液能使酚酞试液变红,滴入酚酞试液后变红的一定是碱溶液 |

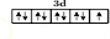 ;
;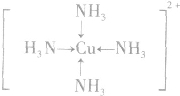 ;名称是四氨合铜离子;[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为平面正方形;
;名称是四氨合铜离子;[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为平面正方形;