题目内容
18.海水是巨大的化学资源宝库.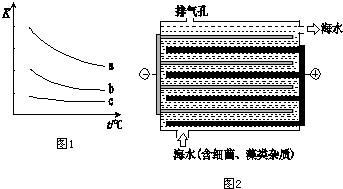
Ⅰ.从海水中可以提取氯、溴、碘等卤族元素.
(1)HClO的电子式是
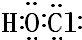 .
.(2)已知:X2 (g)+H2(g)?2HX(g) (X2表示Cl2、Br2和I2).
图1表示平衡常数K与温度t的关系.
①△H 表示X2与H2反应的焓变,则△H<0.(填“>”、“<”或“=”)
②曲线a表示的是I2(填“Cl2”、“Br2”或“I2”)与H2反应时K与t的关系.
Ⅱ.海水淡化具有广泛的应用前景,淡化前需对海水进行预处理.′
(1)通常用明矾[K2SO4•Al2(SO4)3•24H2O]作混凝剂,降低浊度.明矾水解的离子方程式是Al3++3H2O?Al(OH)3(胶体)+3H+.
(2)用图2所示NaClO的发生装置对海水进行消毒和灭藻处理.
①装置中由NaCl转化为NaClO的化学方程式是2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑,2NaOH+Cl2=NaClO+NaCl+H2O.
②海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3.生成CaCO3的离子方程式是Ca2++HCO3-+OH-=CaCO3↓+H2O.
③若每隔5-10min倒换一次电极电性,可有效地解决阴极的结垢问题.试用电极反应式并结合必要的文字进行解释阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e-=Cl2↑,产生的氯气与水发生反应:Cl2+H2O=HCl+HClO,使该电极附近溶液呈酸性,从而将Mg(OH)2和CaCO3溶解而达到除垢的目的.
分析 Ⅰ.(1)次氯酸是共价化合物,氯原子核氢原子与氧原子形成共价键,据此书写电子式;
(2)依据图象分析平衡常数随温度升高减小,说明平衡逆向进行,正反应为放热反应;Cl2、Br2、I2,与H2反应时K与t的关系分析可知氯气和氢气反应放热多;
Ⅱ.(1)明矾中含有铝离子,铝离子在水中水解生成氢氧化铝胶体,胶体具有吸附性而净水;
(2)①电解饱和氯化钠溶液反应生成氢氧化钠、氯气和氢气,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
②阴极生成氢气,水的电离被破坏电极附近生成氢氧化钠,氢氧化钠和碳酸氢钙,碳酸氢镁反应生成氢氧化镁、碳酸钙沉淀;
③阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e-=Cl2↑,产生的氯气与水发生反应:Cl2+H2O=HCl+HClO,酸溶解沉淀.
解答 解:Ⅰ.(1)HClO的电子式是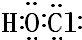 ,故答案为:
,故答案为: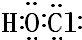 ;
;
(2)①图象分析平衡常数随温度升高减小,说明平衡逆向进行,正反应为放热反应,△H<0,故答案为:<;
②Cl2、Br2、I2,与H2反应时K与t的关系分析可知氯气和氢气反应放热多,碘化氢加热分解平衡逆向进行平衡常数减小的大,曲线a表示的是I2,故答案为:I2;
Ⅱ.(1)明矾中含有铝离子,铝离子在水中水解生成氢氧化铝胶体,胶体具有吸附性而净水,水解方程式为Al3++3H2O?Al(OH)3(胶体)+3H+;
故答案为:Al3++3H2O?Al(OH)3(胶体)+3H+;
(2)①装置中由NaCl转化为NaClO的化学方程式是2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑、2NaOH+Cl2=NaClO+NaCl+H2O,
故答案为:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑;2NaOH+Cl2=NaClO+NaCl+H2O;
②阴极生成氢气,电极附近水的电离被破坏,电极附近生成氢氧化钠,氢氧化钠和碳酸氢钙,碳酸氢镁反应生成氢氧化镁、碳酸钙沉淀,氢氧化钠和碳酸氢钙反应生成CaCO3的沉淀产生水垢,生成碳酸钙沉淀的反应离子方程式是:Ca2++HCO3-+OH-=CaCO3↓+H2O,答案为:Ca2++HCO3-+OH-=CaCO3↓+H2O;
③阴极电解原理分析可知,阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e-=Cl2↑,产生的氯气与水发生反应:Cl2+H2O=HCl+HClO,使该电极附近溶液呈酸性,从而将Mg(OH)2和CaCO3溶解而达到除垢的目的,
故答案为:阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e-=Cl2↑,产生的氯气与水发生反应:Cl2+H2O=HCl+HClO,使该电极附近溶液呈酸性,从而将Mg(OH)2和CaCO3溶解而达到除垢的目的.
点评 本题考查了电子式、漂白粉的成份、元素在周期表中位置等,综合性强,学生只要掌握基础是关键,注意离子方程式和电极反应的书写方法应用,题目难度中等.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案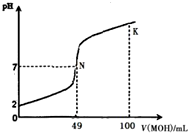 酸碱中和滴定是最基本的定量分析化学实验.常温下,向50mL 0.5mol•L-1 HA溶液中逐滴加入0.5mol•L-1强碱 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述正确的是( )
酸碱中和滴定是最基本的定量分析化学实验.常温下,向50mL 0.5mol•L-1 HA溶液中逐滴加入0.5mol•L-1强碱 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列叙述正确的是( )| A. | 由图中信息可知 HA为强酸,N点为恰好中和 | |
| B. | 常温下一定浓度的 MA稀溶液的pH<7 | |
| C. | K点所对应的溶液中离子浓度的大小关系:c(M+)>c(OH-)>c(A-)>c(H+) | |
| D. | K点对应的溶液中,溶液的pH>13,c(HA)+c(A-)=0.25mol•L-1 |
粗品$→_{操作1}^{饱和NaHSO3溶液}$滤液$→_{萃取}^{乙醛}$操作2有机层$→_{操作3}^{固体干燥剂}$1-丁醇乙醚(操作4)纯品
已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1-丁醇互溶;③1-丁醇的沸点是118℃.则操作1~4分别是( )
| A. | 萃取、过滤、蒸馏、蒸馏 | B. | 过滤、分液、蒸馏、萃取 | ||
| C. | 过滤、蒸馏、过滤、蒸馏 | D. | 过滤、分液、过滤、蒸馏 |
| 实验序号 | 金属 质量/g | 金属状态 | c(H2SO4) /mol•L-1 | V(H2SO4)/mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
(1)由实验可推知,反应物的总能量>产物的总能量(填“<““>““一“).
(2)实验4和5表明,固体反应物的表面积 对反应速率有影响,能表明同一规律的实验还有 (填实验序号);
(3)仅表明反应物浓度对反应速率产生影响的实验有l、3、4、6、8及2、5(填实验序号);
(4)本实验中影响反应速率的其他因素还有反应温度,其实验序号是6和7或8和9.
| A. | 按系统命名法,化合物 的名称为2,6-二甲基-5-乙基庚烷 的名称为2,6-二甲基-5-乙基庚烷 | |
| B. | 乙烯和聚乙烯二者都能使溴的四氯化碳溶液褪色 | |
| C. | 化合物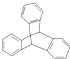 是苯的同系物 是苯的同系物 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
| A. | 标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA | |
| B. | 0.5molC3H8分子中所含C-H共价键数为2NA | |
| C. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| D. | 1mol碳正离子CH3+所含的电子数为6NA |
| A. | 酯基的官能团符号:-COO- | B. | 硝基苯的结构简式: | ||
| C. | COCl2分子的结构式: | D. | 乙炔的电子式: |
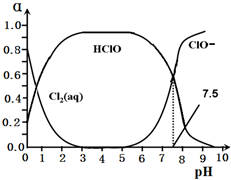 元素周期表中ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中ⅦA族元素的单质及其化合物的用途广泛.