题目内容
往含0.2mol NaOH和0.1mol Ba(OH)2的溶液中持续稳定地通入CO2气体,当通入气体的体积为6.72L(标准状况下)时立即停止,则在这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图象是(气体的溶解忽略不计)
A. B.
B. C.
C. D.
D.
汽车尾气排放的NO和CO都是有毒的气体,科学家正在研究利用催化技术将尾气中的NO和CO转变成无毒的CO2和N2,减少污染。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.0 kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol
2C(s)+2O2(g)=2CO2(g) △H=-787.0 kJ/mol
则尾气转化反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=
N2(g)+2CO2(g) △H=  。
。
(2)对于反应2NO(g)+2CO(g) N2(g)+2CO2(g),为了测定
N2(g)+2CO2(g),为了测定 在某种催化剂作用下的
在某种催化剂作用下的 反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/×10-4 mol/L | 3.00 | 2.25 | 1.75 | 1.36 | 1.00 | 1.00 |
c(CO)/×10-4 mol/L | 4.00 | 3.25 | 2.75 | 2.36 | 2.00 | 2.00 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率 υ(CO2)= mol/(L•s)。
②在该温度下,反应的平衡常数K= 。
(3)假设在恒容密闭容器中发生上述反应,下列有关说法正确的是 。
A.选用更有效的催化剂能提高尾气的转化率
B.升高反应体系的温度能提高反应速率, 提高尾气的转化率
C.相同温度下,若NO和CO的起始浓度分别为1.50×10-4 mol/L和2.00×10-4 mol/L,平衡时N2的体积分数比原平衡体系中N2的体积分数低
D.单位时间内消耗NO的物质的量等于生成CO2的物质的量时即达平衡状态
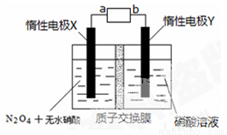
(4)用尾气NO2为原料可制新型硝化剂N2O5,原理:先将NO2转化为N2O4,再采用电解法制备N2O5,装置如右图所示则电源b极是__________极(填“正”“负”),生成N2O5电极反应式为 ,电解一段时间后硝酸溶液的pH (填“增大”“减小”“不变”)。


 入到稀硝
入到稀硝 酸中,金属完全溶解(假设反应中还原产物全部是NO)。向反
酸中,金属完全溶解(假设反应中还原产物全部是NO)。向反 应后的溶液中加入3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加7.65g,则下列叙述中正确的是( )
应后的溶液中加入3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加7.65g,则下列叙述中正确的是( ) OH溶液的
OH溶液的 体积为150mL
体积为150mL 金属的总质量一定是9.9g
金属的总质量一定是9.9g

 Cl
Cl
