题目内容
7.下列叙述正确的是( )| A. | pH试纸使用之前需用蒸馏水润湿 | |
| B. | 用广泛pH试纸测定某溶液的pH为3.5 | |
| C. | pH=7的溶液一定呈中性 | |
| D. | 中性溶液的c(H+)=$\sqrt{K_W}$mol•L-1 |
分析 c(H+)与c(OH-)的相对大小可判定溶液的酸碱性,且Kw与温度有关,测定pH时试纸不能润湿,以此来解答.
解答 解:A.pH试纸使用之前不能用蒸馏水润湿,否则可能有误差,故A错误;
B.用广泛pH试纸测定某溶液的pH为3或4,为正整数,故B错误;
C.pH=7的溶液不一定呈中性,如100℃pH=6为中性,故C错误;
D.c(H+)=$\sqrt{K_W}$mol•L-1,即c(H+)=c(OH-),溶液为中性,故D正确;
故选D.
点评 本题考查溶液的酸碱性,为高频考点,把握酸碱性的判断方法、pH与酸碱性的关系为解答的关键,侧重分析与应用能力的考查,注意pH的测定方法,题目难度不大.

练习册系列答案
相关题目
18.某种兴奋剂的结构简式如图所示,有关该物质的说法错误的是( )
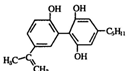

| A. | 该有机物不仅能使溴水、酸性 KMnO4 溶液褪色,也能与FeCl3溶液发生显色反应 | |
| B. | 一定条件下该有机物能发生加成反应、氧化反应、取代反应,也能发生聚合反应 | |
| C. | 该有机物中可能存在手性碳原子 | |
| D. | 该有机物显弱酸性,能与 NaOH 溶液、NaHCO3 溶液发生反应 |
19.下列属于酸性氧化物的是( )
| A. | Ca(OH)2 | B. | SiO2 | C. | Na2O | D. | H2SO4 |
16.分子式为C5H12O,能发生催化氧化生成醛,符合此要求的醇的种类为( )
| A. | 3种 | B. | 4 种 | C. | 5 种 | D. | 8种 |
20.某学生为了探究Zn与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的Zn粉,用排水集气法收集反应放出的H2,实验记录如下(累计值):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3,你认为原因是该反应是放热反应,2~3min时温度高,温度对反应速率影响占主导作用.
(2)4~5min时间段的反应速率最小,你认为原因是4~5min时H+浓度小,浓度对反应速率影响占主导作用.
(3)求2~3min时间段内以盐酸的浓度变化来表示的反应速率(假设溶液体积保持不变)V(HCl)=0.1mol/(L•min).
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O B.NaCl溶液 C.Na2CO3溶液 你认为可行的是(填编号)AB.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况下) | 50 | 120 | 232 | 290 | 310 |
(2)4~5min时间段的反应速率最小,你认为原因是4~5min时H+浓度小,浓度对反应速率影响占主导作用.
(3)求2~3min时间段内以盐酸的浓度变化来表示的反应速率(假设溶液体积保持不变)V(HCl)=0.1mol/(L•min).
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O B.NaCl溶液 C.Na2CO3溶液 你认为可行的是(填编号)AB.
