题目内容
12.通常人们把拆开1mol化学键吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热.下列是一些化学键的键能.| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | 放热1940kJ | B. | 吸热1940kJ | C. | 放热485kJ | D. | 吸热485kJ |
分析 焓变为反应物中键能之和减去生成物中键能之和,以此来解答.
解答 解:由表格中数据及CH4+4F2═CF4+4HF可知,△H=(414kJ/mol)×4+(155kJ/mol)×4-(489kJ/mol)×4-(565kJ/mol)×4=-1940kJ/mol,则每消耗1molCH4的热效应为放热1940kJ,
故选A.
点评 本题考查反应热与焓变,为高频考点,把握反应物能量变化、焓变与键能的关系为解答本题关键,侧重分析与应用能力的考查,注意焓变为负时反应为放热反应,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
3.下列能够检验出KI中是否含有Br-的实验是( )
| A. | 加入足量的新制氯水,溶液变色则有Br- | |
| B. | 加入酸性KMnO4溶液,观察溶液颜色是否褪去 | |
| C. | 加入硝酸银溶液,再加稀硝酸,若有浅黄色沉淀则有Br- | |
| D. | 加入足量FeCl3溶液,用CCl4萃取后,在无色的水层中加入氯水,溶液呈橙黄色,则含有Br- |
3.下列有关叙述不正确的是( )
| A. | 一个D2O分子中所含中子数为8 | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<HNO3 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
20.我国鼓励沿海省市建设海洋强省.下列说法不正确的是( )
| A. | 从海带中提取碘单质的过程涉及氧化还原反应 | |
| B. | 往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输 | |
| C. | 赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的 | |
| D. | 从海水中获得食盐和淡水必须经过化学反应 |
7.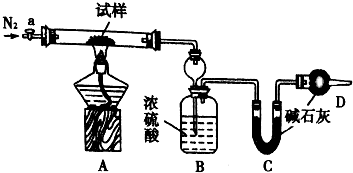 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.
实验过程:
I.按图组装仪器,检查装置的气密性;
II.将m1 g试样放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3 g;
Ⅲ,关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;Ⅳ.称得装置B的质量为m4g、装置C的质量为m5g.
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O.
(2)装置B的作用为吸收反应生成的水蒸气.装置C的作用为吸收反应生成的二氧化碳.
(3)实验过程中通入N2的目的为使装置中的二氧化碳和水蒸气全部排出被装置BC全部吸收.
(4)用下列各项所提供的数据能计算出NaHCO3的质量分数w(NaHCO3)的是bce(填选项字母)
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3),若能,则w(NaHCO3)的计算式为:$\frac{42({m}_{5}-{m}_{3})}{11{m}_{1}}$×100%(若不能,此问不作答.)
 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.实验过程:
I.按图组装仪器,检查装置的气密性;
II.将m1 g试样放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3 g;
Ⅲ,关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;Ⅳ.称得装置B的质量为m4g、装置C的质量为m5g.
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O.
(2)装置B的作用为吸收反应生成的水蒸气.装置C的作用为吸收反应生成的二氧化碳.
(3)实验过程中通入N2的目的为使装置中的二氧化碳和水蒸气全部排出被装置BC全部吸收.
(4)用下列各项所提供的数据能计算出NaHCO3的质量分数w(NaHCO3)的是bce(填选项字母)
| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
4.下列化学反应属于吸热反应的是( )
| A. | 盐酸与烧碱溶液的反应 | B. | Al与稀盐酸的反应 | ||
| C. | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO | D. | 葡萄糖在人体内氧化分解 |
1.一定条件下的反应:PCl5(g)?PCl3(g)+Cl2(g)△H>0.达到平衡后,下列情况使PCl5分解率降低的是( )
| A. | 温度不变,增大容器体积 | B. | 体积不变,对体系加热 | ||
| C. | 温度和体积不变,充入氩气 | D. | 温度和体积不变,充入氯气 |
2.仅用如图装置可完成( )


| A. | 浓硫酸和铜制SO2 | B. | 用Cu与浓HNO3反应制NO2 | ||
| C. | 用 NH4Cl 与 Ca(OH)2反应制 NH3 | D. | 用锌粒与稀H2SO4反应制H2 |