题目内容
17.目前,世界上多采用电解熔融氯化钠的方法来生产金属钠:2NaCl(熔融)$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2.己知物质A、B、C、D、E、F 有如图所小转化关系: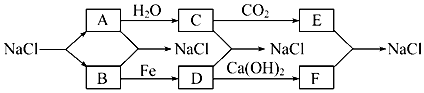
(1)试根据上述变.化写出A、B、C、D、E、F 的化学式:
ANa,BCl2,CNaOH,DFeCl3,ENa2CO3,FCaCl2.
(2)请写出A→C 以及B→D 两个反应的化学方程式.
①A→C2Na+2H2O=2NaOH+H2↑,②B→D2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(3)过氧化钠可用作制氧剂,写出过氧化钠与二氧化碳反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
(4)工业上制取漂白粉的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
分析 由2NaCl(熔融)$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2,且A与B反应生成NaCl,B与Fe反应生成D,可知A为Na,B为Cl2,结合图中转化可知C为NaOH,E为Na2CO3,D为FeCl3,FeCl3与氢氧化钙反应生成F为CaCl2,E与F反应生成碳酸钙和NaCl,以此来解答.
解答 解:(1)由上述分子可知,A、B、C、D、E、F分别为Na、Cl2、NaOH、FeCl3、Na2CO3、CaCl2,
故答案为:Na;Cl2;NaOH;FeCl3;Na2CO3; CaCl2;
(2)①A→C的反应为2Na+2H2O=2 NaOH+H2↑,②B→D的反应为2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$ 2FeCl3,
故答案为:2Na+2H2O=2 NaOH+H2↑;2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$ 2FeCl3;
(3)过氧化钠与二氧化碳反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)工业上制取漂白粉的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
点评 本题考查无机物的推断,为高频考点,把握图中转化、电解原理、元素化合物知识为解答本题关键,侧重分析与推断能力的考查,注意化学用语的使用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列说法中正确的是( )
| A. | 书写共价化合物的电子式只需把结构式中的一个单键改成一对电子即可 | |
| B. | 已知  ,可见,成键的一方不提供电子也可能形成化学键 ,可见,成键的一方不提供电子也可能形成化学键 | |
| C. | 将某种化合物溶于水,若能导电说明这种化合物是离子化合物 | |
| D. | 只要是离子化合物其熔点就比共价化合物的熔点高 |
12.通常人们把拆开1mol化学键吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热.下列是一些化学键的键能.
根据键能数据估算反应CH4+4F2═CF4+4HF每消耗1molCH4的热效应( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | 放热1940kJ | B. | 吸热1940kJ | C. | 放热485kJ | D. | 吸热485kJ |
6.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是( )

| A. | Cl2+2KBr═Br2+2KCl | B. | 2NaHCO3$\frac{\underline{\;△\;}}{\;}$Na2CO3+H2O+CO2↑ | ||
| C. | 3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2 | D. | 2Na2O2+2CO2═2Na2CO3+O2 |

