题目内容
18.已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和直线型分子M (组成E分子的元素的原子序数小于10,组成G分子的元素为第三周期的元素).如图,则下列判断中正确的是( )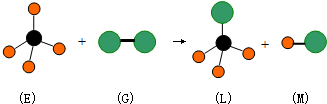
| A. | L能溶于水 | B. | M属于离子化合物 | ||
| C. | G有漂白性 | D. | 该反应是取代反应 |
分析 正四面体形分子E,组成E分子的元素的原子序数都小于10,E由两种元素组成,红色球只形成一个共价键,所以是H元素,黑色球表示C元素,所以E是甲烷;直线型分子G,组成G分子的元素为第三周期的元素,且G是双原子分子,所以G是Cl元素,该反应是甲烷和氯气发生取代反应生成一氯甲烷和氯化氢,即L是一氯甲烷,M是氯化氢.
A.卤代烃不溶于水;
B.一般来说,活泼金属和活泼非金属元素之间存在离子键,非金属元素之间易形成共价键,离子化合物中一定含有离子键,共价化合物中只含共价键;
C.氯气没有漂白性;
D.有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应;有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应.
解答 解:正四面体形分子E,组成E分子的元素的原子序数都小于10,E由两种元素组成,红色球只形成一个共价键,所以是H元素,黑色球表示C元素,所以E是甲烷;直线型分子G,组成G分子的元素为第三周期的元素,且G是双原子分子,所以G是Cl元素,该反应是甲烷和氯气发生取代反应生成一氯甲烷和氯化氢,即L是一氯甲烷,M是氯化氢.
A.常温常压下,一氯甲烷是气体,不溶于水,故A错误;
B.氯化氢中只含共价键,属于共价化合物,故B错误;
C.氯气没有漂白性,但次氯酸有漂白性,故C错误;
D.甲烷中的氢原子被氯原子取代生成一氯甲烷,属于取代反应,故D正确;
故选D.
点评 本题以物质的推断为载体考查了元素化合物的性质、有机反应等知识点,能正确推断物质是解本题的关键,注意卤代烃不溶于水.

练习册系列答案
相关题目
8.某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或二种,现将13.8克样品加入足量水,样品全部溶解;再加入过量的CaCl2溶液,得到9克沉淀. 对样品所含杂质的正确判断是( )
| A. | 肯定有KNO3,肯定没有Na2CO3 | B. | 肯定没有Ba(NO3)2,可能有KNO3 | ||
| C. | 肯定有KNO3,可能还有Na2CO3 | D. | 肯定没有Na2CO3和Ba(NO3)2 |
13.家用液化石油气的主要成份是( )
| A. | 甲烷和乙烷 | B. | 丙烷和丁烷 | C. | 乙烷和乙烯 | D. | 戊烷和己烷 |
10.下列物质的用途中,利用物质氧化性的是( )
| A. | 次氯酸消毒餐具 | B. | 氧化铝做耐火材料 | ||
| C. | 焦炭用于炼铁工业 | D. | K、Na合金作原子反应堆导热剂 |
7.可用于检验乙醇中是否有水的试剂是( )
| A. | 无水硫酸铜 | B. | 石灰石 | C. | 金属钠 | D. | 胆矾 |
8.不饱和度Ω是表示有机物结构的重要参数,不饱和度指相对链状烷烃分子,有机物分子中缺氢程度.每缺2个氢原子,该有机分子的不饱和度为1.例如,乙烯、乙炔、苯的不饱和度分别为1、2、4,环己烷、乙醛、乙酸的不饱和度为1.下列推断正确的是( )
| A. | C5H8分子可能含1个碳碳三键或2个碳碳双键,或1个环和1个碳碳双键,或2个环 | |
| B. | C7H16O可能含1个碳碳双键或1个碳氧双键 | |
| C. | C5H10O2可能含1个碳碳双键和1个碳氧双键,或2个碳氧双键 | |
| D. | C8H10O一定是芳香族化合物 |
 .
.