题目内容
8.某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或二种,现将13.8克样品加入足量水,样品全部溶解;再加入过量的CaCl2溶液,得到9克沉淀. 对样品所含杂质的正确判断是( )| A. | 肯定有KNO3,肯定没有Na2CO3 | B. | 肯定没有Ba(NO3)2,可能有KNO3 | ||
| C. | 肯定有KNO3,可能还有Na2CO3 | D. | 肯定没有Na2CO3和Ba(NO3)2 |
分析 现将13.8克样品加入足量水,样品全部溶解,则不可能含有Ba(NO3)2,加入氯化钙能产生沉淀,然后根据沉淀的质量进一步确定碳酸钠和硝酸钾的存在.
解答 解:解:样品加入水中,全部溶解,说明一定无硝酸钡,若13.8 g样品全是K2CO3,样品溶解后,加入过量的CaCl2溶液,
K2CO3+CaCl2═CaCO3↓+2KCl
138 100
13.8g x
x=$\frac{13.8g×100}{138}$=10g,
而Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
13.8g y
y=$\frac{13.8g×100}{106}$=13g,
现得到9g沉淀,则等质量的杂质与CaCl2溶液作用得到的沉淀小于10g,
所以样品中肯定有KNO3,可能还有Na2CO3,
故选C.
点评 本题考查了混合物反应的计算,题目难度不大,明确发生反应的实质为解答关键,注意掌握极值法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.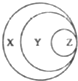 图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )
图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )
 图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )
图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )| 选项 | X | Y | Z |
| A | 胶体 | 混合物 | 淀粉溶液 |
| B | 化合物 | 酸性氧化物 | 一氧化氮 |
| C | 气态氢化物 | 化合物 | 液溴 |
| D | 强电解质 | 强酸 | 硫酸 |
| A. | A | B. | B | C. | C | D. | D |
16.下列关于化学键的叙述正确的是( )
| A. | 离子化合物一定不含共价键 | B. | 化学键的形成与原子结构无关 | ||
| C. | 共价键只存在于共价化合物中 | D. | 离子键只存在于离子化合物中 |
13.下列装置能达到实验目的是( )
| A. | 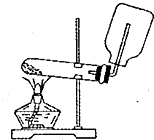 实验室制取并收集氨气 | B. | 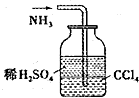 吸收氨气 | ||
| C. | 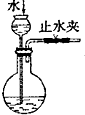 代替启普发生器 | D. | 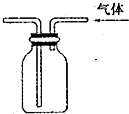 排空气法收集二氧化碳 |
20.联合国卫生组织经过考核和研究,认为我国使用的铁锅是有益于人类健康的理想炊具,并向全世界推广.其主要原因是( )
| A. | 价格便宜,不易生锈 | |
| B. | 铁锅含有碳元素 | |
| C. | 烹调的食物中留有人体需要的铁元素 | |
| D. | 传热慢,保温性能好 |
17.请选择合适的选项编号填入表格:
除杂可用试剂:
a.碱石灰 b.水 c.浓硫酸 d.饱和食盐水
收集气体方法:
除杂可用试剂:
a.碱石灰 b.水 c.浓硫酸 d.饱和食盐水
收集气体方法:

| 气体 | 所含杂质气体 | 除杂所用试剂 | 收集气体方法(已去除杂质) |
| 氨气 | 水蒸气 | a | B |
| 一氧化氮 | 二氧化氮 | b | A |
18.已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和直线型分子M (组成E分子的元素的原子序数小于10,组成G分子的元素为第三周期的元素).如图,则下列判断中正确的是( )
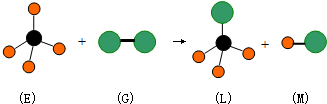

| A. | L能溶于水 | B. | M属于离子化合物 | ||
| C. | G有漂白性 | D. | 该反应是取代反应 |
