��Ŀ����
��¯���������з�������Ҫ��ӦΪ��
![]() Fe2O3(s)��CO(g)
Fe2O3(s)��CO(g)
![]() Fe(s)��CO2(g)
Fe(s)��CO2(g)
��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ������
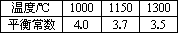
��ش��������⣺
(1)�÷�Ӧ��ƽ�ⳣ������ʽK��________��
(2)��һ���ݻ�Ϊ10 L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0 mol����Ӧ����10 min��ﵽƽ�⣮���ʱ�䷶Χ�ڷ�Ӧ��ƽ����Ӧ����v(CO2)��________��CO��ƽ��ת���ʣ�________��
(3)�����(2)��CO��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��________��
A������Fe����
B������Fe2O3����
C���Ƴ�����CO2
D����߷�Ӧ�¶�
E����С�������ݻ�
F��������ʵĴ���
�𰸣�
������
������
|
����(1)K��c(CO2)/c(CO) ����(2)v(CO2)��0.006 mol/L��min��1 ����CO��ƽ��ת���ʣ�60�� ����(3)C |

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
��¯���������з����ķ�Ӧ��
|
��¯���������з����ķ�Ӧ��
Fe2O3��s��+CO��g��?
Fe��s��+CO2��g������֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����±�������˵������ȷ���ǣ�������
| 1 |
| 3 |
| 2 |
| 3 |
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
| A����H��0 | ||
B���÷�Ӧ��ƽ�ⳣ������ʽ��K=
| ||
| C�������������䣬��ƽ����ϵ����CO2���壬Kֵ��С | ||
| D�������������䣬�����¶ȣ����Խ���CO��ƽ��ת���� |