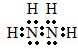题目内容
16.下列分类标准正确的是( )| A. | 化学反应分为:离子反应、非离子反应(标准:是否在水溶液中进行) | |
| B. | 分散系分为:溶液、胶体、浊液(标准:能否透过滤纸) | |
| C. | 化学反应分为:氧化还原反应、非氧化还原反应(标准:元素化合价是否发生变化) | |
| D. | 化合物分为:电解质、非电解质(标准:溶于水或熔融状态能否导电) |
分析 A.有离子参加或离子生成的反应是离子反应;
B.分散系分类依据是微粒直径的大小;
C.氧化还原反应中存在元素化合价的变化;
D.根据电解质的概念分析.
解答 解:A.有离子参加或离子生成的反应是离子反应,在溶液中的反应不一定是离子反应,故A错误;
B.溶液、胶体都可透过滤纸,故B错误;
C.氧化还原反应判断标准应为:是否存在元素化合价的变化,即电子转移,故C正确;
D.在水溶液中或熔融状态下能导电的化合物属于电解质,所以电解质、非电解质的分类标准是:溶于水或熔融状态能否导电,故D正确.
故选CD.
点评 本题考查物质的分类,题目难度不大,注意物质的分类的依据,不同的分类标准会得出不同的分类结果.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.某化学小组准备用环己醇制备环己烯,查得相关资料如下.反应原理: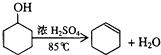
反应物与产物的物理性质:
(1)实验过程中可能发生的有机副反应的方程式为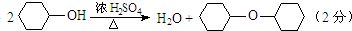 .
.
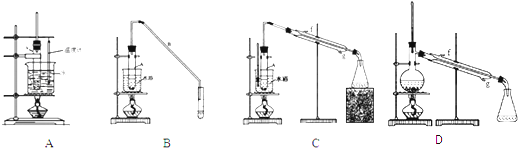
(2)根据上述资料,装置(A,B,C)C最适宜用来完成本次制备实验.
(3)制备粗产品
将5mL环己醇加入试管A中,再加入l0mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全.
(4)粗产品提纯
①环己烯粗产品中含有环己醇和少量酸性杂质等.粗产品需依次经过水洗、加碳酸钠溶液洗涤以及第二次水洗.在此过程中加入碳酸钠溶液的目的是除去环己烯中少量酸性杂质;分液时,环己烯应从分液漏斗的上(填“上”或“下”)口取出.
②向水洗后的环己烯中加入少量的无水氯化钙,再将混合物放入图D所示装置的蒸馏烧瓶(填仪器名称)中,进行蒸馏,收集产品时,温度计显示的温度应为85℃.

反应物与产物的物理性质:
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
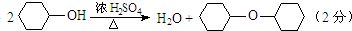 .
.(2)根据上述资料,装置(A,B,C)C最适宜用来完成本次制备实验.

(3)制备粗产品
将5mL环己醇加入试管A中,再加入l0mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全.
(4)粗产品提纯
①环己烯粗产品中含有环己醇和少量酸性杂质等.粗产品需依次经过水洗、加碳酸钠溶液洗涤以及第二次水洗.在此过程中加入碳酸钠溶液的目的是除去环己烯中少量酸性杂质;分液时,环己烯应从分液漏斗的上(填“上”或“下”)口取出.
②向水洗后的环己烯中加入少量的无水氯化钙,再将混合物放入图D所示装置的蒸馏烧瓶(填仪器名称)中,进行蒸馏,收集产品时,温度计显示的温度应为85℃.
7.下列离子方程式中正确的是( )
| A. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 稀硝酸和过量的铁屑反应:3 Fe+8H++2 NO3-=3 Fe3++2 NO↑+4 H2O | |
| D. | 大理石溶于醋酸的反应:CaCO3+CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
11.工业制ClO2的化学反应:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4,下列说法正确的是( )
| A. | NaClO3在反应中化合价降低,失去电子 | |
| B. | SO2在反应中发生氧化反应 | |
| C. | 2mol氧化剂在反应中得到2mol电子 | |
| D. | H2SO4在反应中作氧化剂 |
1.下列描述中正确的是( )
| A. | CS2为V形的极性分子 | |
| B. | ClO3- 的空间构型为平面三角形 | |
| C. | SF6中S原子和氟原子均满足最外层8电子稳定结构 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化,SiF4分子呈空间正四面体,SO32-呈三角锥形 |
8.下列说法正确的是(NA表示阿伏加德罗常数)( )
| A. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| B. | 在常温常压下,11.2升氯气含有的分子数为0.5NA | |
| C. | 在常温常压下,1摩尔气体含有的原子数为NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含原子数目相同 |
5.在同温同压下,两个容积相同的储气瓶,一个装满O2,另一个装满CH4,以下有关两瓶气体的计算不正确的是( )
| A. | O2与CH4质量比为 2:1 | B. | O2与CH4原子数之比为 1:1 | ||
| C. | O2与CH4密度比为2:1 | D. | O2与CH4分子数之比为1:1 |