题目内容
10.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2 L | |
| B. | 25℃,1.01×105 Pa,32 g O2和O3的混合气体所含原子数为2.5NA | |
| C. | 标准状况下,11.2 L H2O含有的原子数为1.5NA | |
| D. | 常温常压下,44 g CO2含有的原子数为3NA |
分析 A、氦气为单原子分子;
B、氧气和臭氧均由氧原子构成;
C、标况下水为液体;
D、求出二氧化碳的物质的量,然后根据二氧化碳中含3个原子来分析.
解答 解:A、氦气为单原子分子,故含NA个氦原子的氦气的物质的量为1mol,故在标况下为22.4L,故A错误;
B、氧气和臭氧均由氧原子构成,故32g混合物中含有的氧原子的物质的量为2mol,个数为2NA个,故B错误;
C、标况下水为液体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、44g二氧化碳的物质的量为1mol,而二氧化碳中含3个原子,故1mol二氧化碳中含3NA个原子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
20.下列应用不涉及氧化还原反应的是( )
| A. | Na2O2用作呼吸面具的供氧剂 | B. | 实验室制二氧化碳 | ||
| C. | 工业上利用合成氨实现人工固氮 | D. | 工业上电解熔融状态Al2O3制备Al |
15.下列有关实验室制取蒸馏水的实验装置与操作的说法中,不正确的是( )
| A. | 实验必须使用温度计,且温度计的水银球应在蒸馏烧瓶的支管口处 | |
| B. | 冷凝管中的水流方向是从下口进入,上口排出 | |
| C. | 实验中需要在蒸馏烧瓶中加入几片碎瓷片,防止出现暴沸现象 | |
| D. | 用酒精灯加热时,蒸馏烧瓶必须垫石棉网 |
19.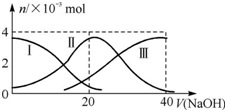 常温下,向20mL 0.2mol•L-1 H2A溶液中滴加0.2mol•L-1 NaOH溶液.有关微粒的物质的量变化如图所示.根据图示判断下列说法正确的是( )
常温下,向20mL 0.2mol•L-1 H2A溶液中滴加0.2mol•L-1 NaOH溶液.有关微粒的物质的量变化如图所示.根据图示判断下列说法正确的是( )
 常温下,向20mL 0.2mol•L-1 H2A溶液中滴加0.2mol•L-1 NaOH溶液.有关微粒的物质的量变化如图所示.根据图示判断下列说法正确的是( )
常温下,向20mL 0.2mol•L-1 H2A溶液中滴加0.2mol•L-1 NaOH溶液.有关微粒的物质的量变化如图所示.根据图示判断下列说法正确的是( )| A. | 当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) | |
| B. | 等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水小 | |
| C. | NaHA溶液中:c(OH-)+c(A2-)=c(H+)+c(H2A) | |
| D. | 向上述加入20 mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减小 |
20.如图所示关于该化合物的下列说法正确的是( )
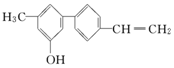

| A. | 完全燃烧时只有二氧化碳和水两种产物 | |
| B. | 由于含有氧元素不是有机物 | |
| C. | 该分子中含有羟基属于醇 | |
| D. | 不能使溴水褪色 |