题目内容
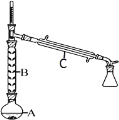
【题目】如图所示为实验室常用装置。回答下列问题:
(1)仪器a的名称为____。
(2)利用二氧化锰与浓盐酸反应制备并收集Cl2时,依次连接装置 A、B、C、D、E并加入适当的 试剂。装置B中饱和食盐水的作用是____;利用装置C干燥Cl2,选用的试剂是____;装置E的作用是____。
(3)利用铜和稀硝酸反应制备并收集NO时,连接装置A、B、E并加入适 当的试剂。A中反应的离子方程式为____,A中导气管应连接B的___(填“b”或“c”)端。实验过程中观察到A中出现了红棕色,但收集的气体为无色,原因是____(用化学方程式表示)。
【答案】分液漏斗 吸收HCl气体 浓硫酸 吸收Cl2 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O c 2NO+O2=2NO2,3NO2+H2O=NO+2HNO3
【解析】
(1)仪器a为分液漏斗;
(2)考查实验室制备Cl2,并收集该气体;
(3)考查实验室制备NO,并收集该气体,需要注意的是,一般使用排水法收集NO。
(1)仪器a为分液漏斗;
(2)实验室制备Cl2,B中装有饱和食盐水,其作用是吸收逸出的HCl气体;C为干燥装置,需要使用浓硫酸;D为收集装置,E为尾气处理装置,用来吸收Cl2;
(3)实验室制备NO,一般使用Cu和稀HNO3,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;收集时由于NO对空气不稳定,一般使用排水法收集,故B中应是装满水的,则A中导气管应连接B的c端;实验过程中观察到A中出现了红棕色,是因为2NO+O2=2NO2,收集的气体为无色,是因为3NO2+H2O=NO+2HNO3。

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案【题目】常用解热镇痛药对乙酰氨基苯酚(扑热息痛)为白色颗粒状晶体,易被空气氧化。实验室用对氨基苯酚乙酰化制备扑热息痛的一种方法如下:

查阅资料获得以下数据:
对氨基苯酚 | 醋酸酐 | 对乙酰氨基苯酚 | |
熔点/℃ | 189.6 ~ 190.2 | -73 | 169 ~ 171 |
密度/g·cm-3 | 1.2 | 1.1 | 1.3 |
相对分子质量 | 109 | 102 | 151 |
溶解性 | 溶于乙醇和水 | 溶于乙醇, 稍溶于水 | 易溶于乙醇和热水,溶于丙酮 |

实验过程:如图所示,在三颈烧瓶中加入对氨基苯酚10.9g,再加入30 mL水。打开仪器a下端的旋塞,缓慢滴加12 mL醋酸酐。搅拌并水浴加热,控制温度在80℃左右,充分反应后按如下流程进行操作。

回答下列问题:
(1)仪器a的名称是___________,仪器b的作用是_____________。
(2)步骤②洗涤晶体获得粗品时,选择的洗涤剂是______。(填标号)
A.乙醇 B.丙酮 C.热水 D.冷水
(3)减压过滤装置如图所示。步骤④减压过滤时,在吸滤瓶中要先加入适量NaHSO3,其作用是_________,该减压过滤需趁热进行,原因是_____________。

(4)步骤⑥中操作X为_______________。
(5)若最终得到9.8 g对乙酰氨基苯酚,则本实验的产率为______%。(保留1位小数)