题目内容
16.将含有0.4molCuSO4和0.4molNaCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上得到0.3mol铜,在另一电极上析出的气体在标准状况下的体积是( )| A. | 5.6L | B. | 6.75L | C. | 13.44L | D. | 11.2L |
分析 电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol<0.4mol,根据转移电子守恒计算阳极上生成气体体积.
解答 解:电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol,阴极上转移电子的物质的量=0.3mol×2=0.6mol,
根据原子守恒知,溶液中n(Cl-)=0.4mol,氯离子完全放电时转移电子的物质的量=0.4mol×1=0.4mol,生成氯气0.2mol;
所以阳极上有氧气生成,电极上电子转移为0.6-0.4=0.2mol,4OH--4e-=2H2O+O2↑,电极反应计算生成氧气0.05mol,所以阳极生成气体物质的量为0.2+0.05=0.25mol,标准状况下气体的体积为0.25×22.4=5.6L,
故选:A.
点评 本题考查了电解原理,明确阴阳极上离子放电顺序是解本题关键,注意要首先根据转移电子相等判断阳极上生成气体成分,再计算其体积,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.工业上常以富含硫酸亚铁的废液为原料生产氧化铁,其主要流程如下:
废液$→_{①}^{提纯、结晶}$FeSO4•7H2O$\stackrel{②}{→}$FeSO4溶液$→_{③}^{NH_{4}HCO_{3}溶液}$FeCO3$\stackrel{④}{→}$Fe2O3
(1)已知步骤①中硫酸亚铁在不同温度下的溶解度和析出晶体的组成如下表所示.
若从硫酸亚铁溶液中结晶出FeSO4•7H2O,控制的温度(t)为t<56.7℃.
(2)步骤②需加一定量硫酸,其主要目的是抑制FeSO4的水解.
(3)生产FeCO3浊液的离子方程式为Fe2++2HCO3-═FeCO3↓+CO2↑+H2O;FeCO3浊液露置在空气中会出现红褐色的固体,该变化的化学方程式为4FeCO3+6H2O+O2═4Fe(OH)3+4CO2.
(4)已知FeSO4•7H2O浊液晶体在加热条件下发生如下反应:FeSO4•7H2O$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑+14H2O↑;利用如图装置可检验该反应的气体产物.
请填写下列空白:
①仪器的连接顺序为a接f(或g)、g(或f)接d、e接h、i接b.
②装置C中的X为氯化钡溶液.
废液$→_{①}^{提纯、结晶}$FeSO4•7H2O$\stackrel{②}{→}$FeSO4溶液$→_{③}^{NH_{4}HCO_{3}溶液}$FeCO3$\stackrel{④}{→}$Fe2O3
(1)已知步骤①中硫酸亚铁在不同温度下的溶解度和析出晶体的组成如下表所示.
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
(2)步骤②需加一定量硫酸,其主要目的是抑制FeSO4的水解.
(3)生产FeCO3浊液的离子方程式为Fe2++2HCO3-═FeCO3↓+CO2↑+H2O;FeCO3浊液露置在空气中会出现红褐色的固体,该变化的化学方程式为4FeCO3+6H2O+O2═4Fe(OH)3+4CO2.
(4)已知FeSO4•7H2O浊液晶体在加热条件下发生如下反应:FeSO4•7H2O$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑+14H2O↑;利用如图装置可检验该反应的气体产物.

请填写下列空白:
①仪器的连接顺序为a接f(或g)、g(或f)接d、e接h、i接b.
②装置C中的X为氯化钡溶液.
4.用NaOH固体配制1.0mol•L-1的NaOH溶液220mL,下列说法正确的是( )
| A. | 首先称取NaOH固体8.8g | |
| B. | 容量瓶中原有少量蒸馏水没有影响 | |
| C. | 定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线 | |
| D. | 定容时仰视刻度线会使所配制的溶液浓度偏高 |
11.下列事实不能用化学平衡移动原理解释的是( )
| A. | 合成氨工业中采用高压条件 | |
| B. | 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 | |
| C. | 用排饱和食盐水的方法收集Cl2 | |
| D. | 在含有[Fe(SCN)]2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
8.下列各组气体中,在通常条件下能稳定共存的是( )
| A. | NH3、HCl | B. | H2S、SO2 | C. | NO、O2 | D. | N2、O2 |
5.下列各装置能够构成原电池的是( )
| A. |  | B. | 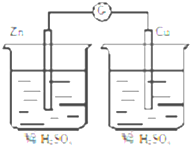 | ||
| C. |  | D. |  |
6.下列关于芳香烃的理解中正确的是( )
| A. | 芳香烃是指分子中含有一个或多个苯环的烃类 | |
| B. | 芳香烃不能使酸性高锰酸钾溶液褪色 | |
| C. | 芳香烃不能与氯气反应 | |
| D. | 芳香烃的所有原子都在同一个平面上 |