题目内容
某次酸雨的分析数据如下:c( )=2.0×10-5mol/L,c(Cl-)=6.0×10-5mol/L,c(Na+)=1.9×10-5mol/L,c(
)=2.0×10-5mol/L,c(Cl-)=6.0×10-5mol/L,c(Na+)=1.9×10-5mol/L,c( )=2.3×10-5mol/L,c(
)=2.3×10-5mol/L,c( )=2.8×10-5mol/L,则此次酸雨的pH大约为
)=2.8×10-5mol/L,则此次酸雨的pH大约为
[ ]
A.3
B.4
C.5
D.6
答案:B
解析:
解析:
|
导解:将酸雨看作溶液,建立电荷守恒的等式:c(Cl-)+2c( |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
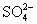 )+c(
)+c( )=c(
)=c( )+c(Na+)+c(H+),因酸雨中c(OH-)浓度值很小,故忽略不计.求出c(H+)=10-4 mol/L.
)+c(Na+)+c(H+),因酸雨中c(OH-)浓度值很小,故忽略不计.求出c(H+)=10-4 mol/L.