题目内容
甲、乙两池电极材料都是铁棒与碳棒(如下图)。请回答下列问题:
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的__________棒;乙池中的__________棒。
②在乙池中阳极的电极反应式是________________________________________。
(2)若两池中均盛放饱和NaCl溶液。
①写出乙池中发生总反应的离子方程式________________________________________。
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5:1,且生成两种酸。该反应的化学方程式为_______________________________________________________。
③若乙池转移0.02 mol电子后停止实验,池中溶液的体积是200 mL,则溶液混匀后的pH=_________。
(1)①碳(C) 铁(Fe)
②4OH--4e-![]() 2H2O+O2↑
2H2O+O2↑
(2)①2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
②5Cl2+I2+6H2O![]() 10HCl+2HIO3
10HCl+2HIO3
③13
解析:甲池为原电池,Fe为负极,C棒为正极;乙池为电解池,Fe为阴极,C棒为阳极.
(1)电解质溶液为CuSO4,两池电极反应:
甲负极:Fe-2e-![]() Fe2+,正极:Cu2++2e-
Fe2+,正极:Cu2++2e-![]() Cu
Cu
乙阴极:Cu2++2e-![]() Cu,阳极:4OH--4e-
Cu,阳极:4OH--4e-![]() O2↑+2H2O.
O2↑+2H2O.
(2)若电解质溶液为NaCl
①乙的总方程式为:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-.
Cl2↑+H2↑+2OH-.
②5Cl2+I2+6H2O![]() 10HCl+2HIO3
10HCl+2HIO3
③由电子守恒可知转移0.02 mol电子,则生成0.02 mol OH-,故c(OH-)=0.1 mol·L-1,则pH=13.

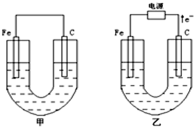 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题: 如图所示,甲、乙两池电极材料都是铁棒和石墨棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和石墨棒,请回答下列问题: 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
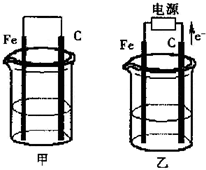 甲、乙两池电极材料都是铁棒与碳棒(如图).请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒(如图).请回答下列问题: