题目内容
15.在8NH3+3Cl2=N2+6NH4Cl反应中,若有标准状态下3.36LCl2参加反应,则被氧化的NH3的质量为( )| A. | 13.6g | B. | 10.2g | C. | 6.8g | D. | 1.7g |
分析 该反应8NH3+3Cl2=6NH4Cl+N2 中Cl元素化合价由0价变为-1价、N元素化合价由-3价变为0价,所以氯气是氧化剂,氯化铵是还原产物,根据氮原子守恒计算被氧化的氨气质量.
解答 解:n(Cl2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,该反应8NH3+3Cl2=6 NH4Cl+N2 中Cl元素化合价由0价变为-1价、N元素化合价由-3价变为0价,由方程式可知,3mol氯气参加反应,可生成1mol氮气,氧化2mol氨气,则0.15mol氯气参加反应,被氧化的氨气的物质的量为0.1mol.质量为0.1mol×17g/mol=1.7g,
故选D.
点评 本题考查了氧化还原反应,明确元素化合价变化是解本题关键,结合基本概念来分析解答,注意只有部分氨气作还原剂,为易错点.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
5.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,6.4g O2和O3的混合气体中含有的原子数为0.4NA | |
| B. | 在反应中消耗0.1molCl2,转移的电子数一定为0.2NA | |
| C. | 含2mol H2SO4的浓硫酸与足量铜粉完全反应,生成气体分子的数目为2NA | |
| D. | 标准状况下,11.2L CCl4中含有的分子数目为0.5NA |
20.一氧化碳、甲醛、二氧化硫均有毒,均是常见的大气污染物.
(1)人们常用催化剂来选择反应进行的方向,如图1为一定条件下1 molCH3OH与O2发生反应时,生成CO或CO2或HCHO的能量变化[反应物O2(g)和生成物H2O(g)已略去].
①在有催化剂的作用下,CH3OH与O2反应的主要产物是HCHO(填“CO”“CO2”或“HCHO”).
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=-470KJ•mol-1.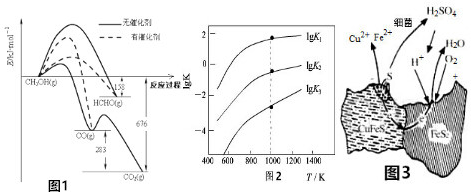
(2)煤炭中的硫主要以黄铁矿的形式存在,用氢气脱出黄铁矿中硫的相关反应见下表,其相关反应的平衡常数的对数值与温度的关系如图2.
①上述反应中,△H1>(填“>”或“<”)0.
②提高硫的脱除率可采取的措施有升高温度(任填一种).
③1000K时,向2L恒容密闭容器中充入一定量的H2(g)和FeS2(g),只发生反应①,达到平衡时,H2的转化率为99%.
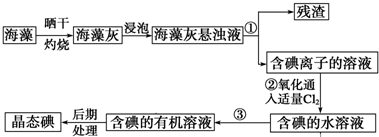
(3)用细菌冶炼铜时,当黄铜矿中伴有黄铁矿时,可明显提高浸取速率,其原理如图3.
①冶炼过程中,正极周围溶液的pH增大(填“增大”“减小”或“不变”).
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
(1)人们常用催化剂来选择反应进行的方向,如图1为一定条件下1 molCH3OH与O2发生反应时,生成CO或CO2或HCHO的能量变化[反应物O2(g)和生成物H2O(g)已略去].
①在有催化剂的作用下,CH3OH与O2反应的主要产物是HCHO(填“CO”“CO2”或“HCHO”).
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=-470KJ•mol-1.

(2)煤炭中的硫主要以黄铁矿的形式存在,用氢气脱出黄铁矿中硫的相关反应见下表,其相关反应的平衡常数的对数值与温度的关系如图2.
| 相关反应 | 反应热 | 平衡常数K |
| ①FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| ②$\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$FeS(s)+H2S(g) | △H2 | K2 |
| ③FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(任填一种).
③1000K时,向2L恒容密闭容器中充入一定量的H2(g)和FeS2(g),只发生反应①,达到平衡时,H2的转化率为99%.
(3)用细菌冶炼铜时,当黄铜矿中伴有黄铁矿时,可明显提高浸取速率,其原理如图3.
①冶炼过程中,正极周围溶液的pH增大(填“增大”“减小”或“不变”).
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
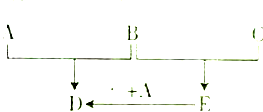 已知A、B、C为常见单质,在一定条件下可发生如下转化(反应条件及部分反应物和生成物已省略):
已知A、B、C为常见单质,在一定条件下可发生如下转化(反应条件及部分反应物和生成物已省略):

 ),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N原子在同一周期(或电子层数相同),N原子核电荷数更大,原子半径更小,原子核对外层电子的吸引力更强.
),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N原子在同一周期(或电子层数相同),N原子核电荷数更大,原子半径更小,原子核对外层电子的吸引力更强.