题目内容
(1) NH3+ O2
NO+ H2O.该反应中氧化剂是 ,被氧化的元素是 ,氧化产物是 ;
(2)若有1molO2参加,则反应中转移电子是 mol.
(3)配平该反应方程式并用单线桥标出电子转移的方向和数目.
| ||
| △ |
(2)若有1molO2参加,则反应中转移电子是
(3)配平该反应方程式并用单线桥标出电子转移的方向和数目.
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应中N元素化合价由-3价升高到+2价,O元素化合价由0价降低到+2价,反应中O2为氧化剂,NH3为还原剂,结合化合价的变化解答该题.
解答:
解:(1)反应中O元素得电子,化合价降低,N元素失电子,化合价升高,被氧化,反应的方程式为4NH3+5O2
4NO+6H2O,反应中O2为氧化剂,NH3为还原剂,氧化产物为NO,
故答案为:4;5;4;6;O2;N;NO;
(2)反应中O元素化合价由0价降低到-2价,若有1molO2参加,则反应中转移电子是4mol,故答案为:4;
(3)反应中O元素得电子,化合价降低,N元素失电子,化合价升高,转移电子数目为20,电子转移的方向和数目可表示为 ,
,
故答案为: .
.
| ||
| △ |
故答案为:4;5;4;6;O2;N;NO;
(2)反应中O元素化合价由0价降低到-2价,若有1molO2参加,则反应中转移电子是4mol,故答案为:4;
(3)反应中O元素得电子,化合价降低,N元素失电子,化合价升高,转移电子数目为20,电子转移的方向和数目可表示为
 ,
,故答案为:
 .
.
点评:本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高频考点,注意从元素化合价的角度解答该题,难度不大,注意相关基础知识的积累.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
工业生产中物质制备时,通过下列反应原理一步完成获得产物、符合“绿色化学”原则的反应是( )
| A、化合反应 | B、分解反应 |
| C、复分解反应 | D、置换反应 |
下列叙述正确的是( )
| A、等质量的铝分别与足量氢氧化钠溶液和稀硝酸反应,放出的氢气一样多 |
| B、将SO2通入过量Ba(NO3)2溶液可生成BaSO4沉淀 |
| C、自来水厂常用明矾对水进行杀菌、消毒 |
| D、将稀硫酸滴加到Fe(NO3)2溶液中无明显现象 |
用胆矾(CuSO4?5H2O)晶体配制0.1mol/L的CuSO4溶液500mL,下列方法正确的是( )
| A、称取8.0g胆矾使其溶于500mL水中 |
| B、称取12.5g胆矾使其溶于500mL水中 |
| C、称取12.5g胆矾使其溶于适量水中,再加水稀释至500mL. |
| D、称取8.0g胆矾使其溶于375g水中 |
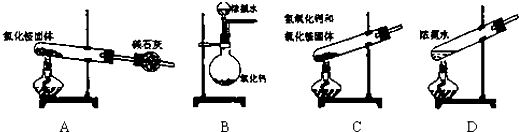
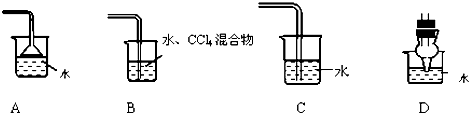
以下实验装置一般不用于分离物质的是( )
A、 |
B、 |
C、 |
D、 |
下列各种材料属于有机合成材料的是( )
| A、用于制作人造卫星天线的钛-镍形状记忆合金 |
| B、用于制作纳米陶瓷材料的氮化硼 |
| C、用于制作灯饰外壳材料的聚苯乙烯塑料 |
| D、用于制作飞机机翼、火箭锥头的碳纤维材料 |
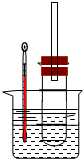 溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物.
溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物.