题目内容
下列叙述正确的是( )
| A、等质量的铝分别与足量氢氧化钠溶液和稀硝酸反应,放出的氢气一样多 |
| B、将SO2通入过量Ba(NO3)2溶液可生成BaSO4沉淀 |
| C、自来水厂常用明矾对水进行杀菌、消毒 |
| D、将稀硫酸滴加到Fe(NO3)2溶液中无明显现象 |
考点:铝的化学性质,胶体的重要性质,二氧化硫的化学性质,二价Fe离子和三价Fe离子的检验
专题:
分析:A、铝和稀硝酸反应不生成氢气;
B、发生氧化还原反应生成硫酸钡、NO、水;
C、明矾净水的原理是:明矾电离的Al3+水解生成Al(OH)3胶体,具有吸附性,将悬浮物沉降,明矾不具有杀菌消毒的作用;
D、酸性条件下,亚铁离子被硝酸根离子氧化生成铁离子.
B、发生氧化还原反应生成硫酸钡、NO、水;
C、明矾净水的原理是:明矾电离的Al3+水解生成Al(OH)3胶体,具有吸附性,将悬浮物沉降,明矾不具有杀菌消毒的作用;
D、酸性条件下,亚铁离子被硝酸根离子氧化生成铁离子.
解答:
解:A、因为铝和稀硝酸反应不生成氢气,故A错误;
B、硝酸盐在酸性条件具有强氧化性,则发生氧化还原反应生成硫酸钡、NO、水,故B正确;
C、明矾只能净水不具有杀菌消毒的作用,故C错误;
D、酸性条件下,亚铁离子被硝酸根离子氧化生成铁离子,所以溶液颜色由浅绿色变为黄色,故D错误
故选B.
B、硝酸盐在酸性条件具有强氧化性,则发生氧化还原反应生成硫酸钡、NO、水,故B正确;
C、明矾只能净水不具有杀菌消毒的作用,故C错误;
D、酸性条件下,亚铁离子被硝酸根离子氧化生成铁离子,所以溶液颜色由浅绿色变为黄色,故D错误
故选B.
点评:本题考查元素化合物的基本性质,侧重于考查学生的综合运用化学知识的能力和评价能力,题目难度不大,注意把握相关物质的性质及物质的结构.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
国际巴黎车展示上,世界各大汽车商纷纷推出环保动力小汽车,使用的新型环保电池为( )
| A、氢氧燃料电池 | B、锌锰电池 |
| C、镍镉电池 | D、铅蓄电池 |
实验中需1mol/L的NaOH溶液950mL,配制时应选用的容量瓶的规格和称取NaOH的质量分别是( )
| A、1000mL,38.0g |
| B、1000mL,40.0g |
| C、任意规格,38.0g |
| D、500mL,20.0g |
下列说法正确的是( )
| A、用氨水鉴别Al3+、Mg2+、Ag+ |
| B、向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为血红色,该溶液中不一定含有Fe2+ |
| C、NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用烧碱溶液就可把它们鉴别开来 |
| D、要证明Fe3+溶液中含有Fe2+可以用NH4SCN溶液和氯水 |
下列图标是国家节水标志的是( )
A、 |
B、 |
C、 |
D、 |
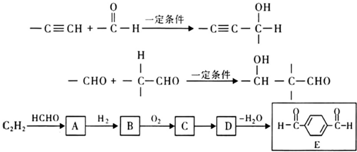
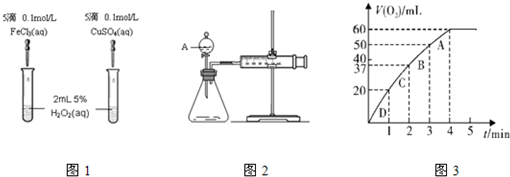
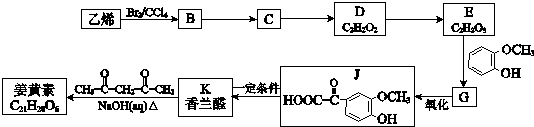
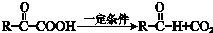
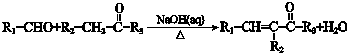 (R1、R2、R3为烃基或氢原子)
(R1、R2、R3为烃基或氢原子)