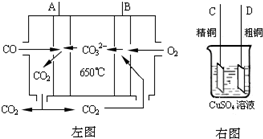
题目内容
利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍.Ni(s)+4CO(g)
Ni(CO)4(g)△H<0,下列说法正确的是( )
| 50-80℃ |
| 180-200℃ |
| A、50~80℃时,适当增大压强,有利于Ni(CO)4的生成 | ||
| B、利用上述原理提纯粗镍需要消耗大量的CO气体 | ||
| C、50~200℃范围内,该反应的平衡常数随温度的升高而减小 | ||
D、该反应的平衡常数表达式是K=
|
分析:A.增大压强,平衡向气体体积减小的方向移动;
B.提纯过程中CO可以循环利用;
C.正反应放热,升高温度,平衡向逆反应方向移动;
D.平衡常数中不出现固体.
B.提纯过程中CO可以循环利用;
C.正反应放热,升高温度,平衡向逆反应方向移动;
D.平衡常数中不出现固体.
解答:解:A.50~80℃时正反应是气体体积减小的反应,增大压强,平衡向正反应方向移动,有利于Ni(CO)4的生成,故A正确;
B.50~80℃CO为反应物,180~200℃时CO为生成物,CO可以循环利用,无需消耗大量的CO,故B错误;
C.正反应放热,升高温度,平衡向逆反应方向移动,该反应的平衡常数随温度的升高而减小,故C正确;
D.该反应的平衡常数表达式是K=
,故D错误.
故选AC.
B.50~80℃CO为反应物,180~200℃时CO为生成物,CO可以循环利用,无需消耗大量的CO,故B错误;
C.正反应放热,升高温度,平衡向逆反应方向移动,该反应的平衡常数随温度的升高而减小,故C正确;
D.该反应的平衡常数表达式是K=
| c[Ni(CO)4] |
| c4(CO) |
故选AC.
点评:本题考查外界条件对化学平衡的影响,侧重于学生的分析能力的考查,为高频考点,难度不大,本题注意控制的温度不同,发生的反应不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H
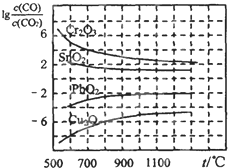 一氧化碳是一种用途相当广泛的化工基础原料.
一氧化碳是一种用途相当广泛的化工基础原料. Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H