题目内容
下列反应中属于氧化还原反应的是( )
分析:根据反应中是否存在元素的化合价变化来判断是否为氧化还原反应,若有元素的化合价变化,则属于氧化还原反应.
解答:解:A、CO2+H2O═H2CO3中各元素的化合价在反应前后都没有变化,则属于非氧化还原反应,故A不选;
B、H2CO3═CO2↑+H2O中各元素的化合价在反应前后都没有变化,则属于非氧化还原反应,故B不选;
C、CaCO3+2HCl═CaCl2+H2O+CO2↑中各元素的化合价在反应前后都没有变化,则属于非氧化还原反应,故C不选;
D、CO2+C
2CO中C元素的化合价由+4价降低为+2价,C元素的化合价由0升高到+2价,则属于氧化还原反应,故D选;
故选D.
B、H2CO3═CO2↑+H2O中各元素的化合价在反应前后都没有变化,则属于非氧化还原反应,故B不选;
C、CaCO3+2HCl═CaCl2+H2O+CO2↑中各元素的化合价在反应前后都没有变化,则属于非氧化还原反应,故C不选;
D、CO2+C
| ||
故选D.
点评:本题考查氧化还原反应的判断,较简单,熟悉常见元素的化合价,并准确判断元素在反应前后的物质中的化合价及是否变化即可解答.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
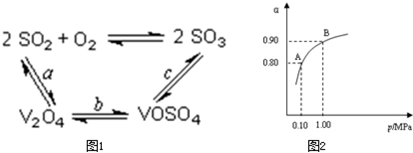
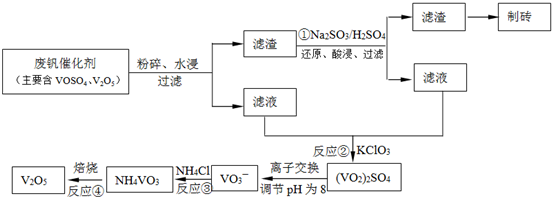
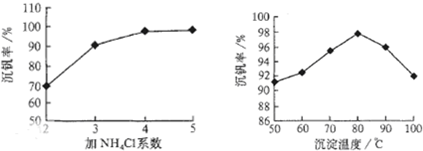
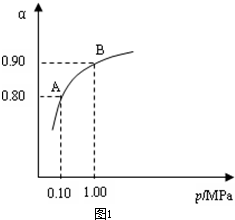 工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题:
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题: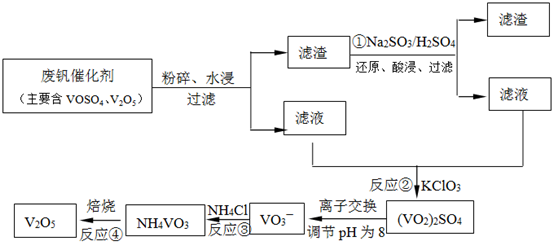
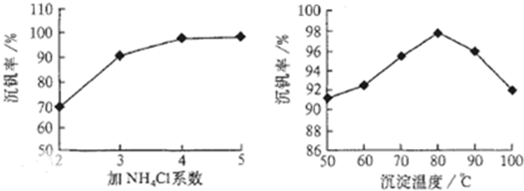






 2SO3(g);△H<0
2SO3(g);△H<0

