题目内容
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题:
(1)煅烧黄铁矿形成的炉气必须经除尘、洗涤、干燥后进入______(填设备名称),其主要目的是______.
(2)催化氧化所使用的催化剂钒触媒(V2O5)能加快二氧化硫氧化速率,此过程中产生了一连串的中间体(如图1).其中a、c二步的化学方程式可表示为:______、______.
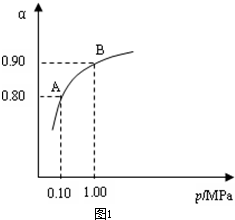
(3)550℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图2所示.则:将2.0mol SO2和1.0mol O2置于5L密闭容器中,反应达平衡后,体系总压强为0.10M Pa.该反应的平衡常数等于______.A与B表示不同压强下的SO2转化率,通常情况下工业生产中采用常压的原因是______.
(4)为循环利用催化剂,科研人员最新研制了一种离子交换法回收钒的新工艺,
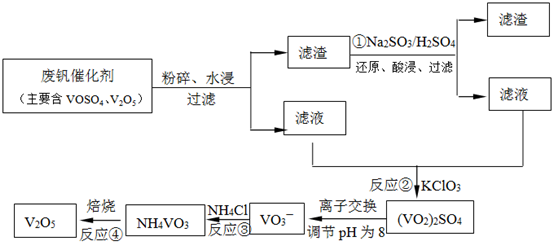
回收率达91.7%以上.已知废钒催化剂中含有V2O5、VOSO4及不溶性残渣.查阅资料知:VOSO4可溶于水,V2O5难溶于水,NH4VO3难溶于水.该工艺的流程如图.
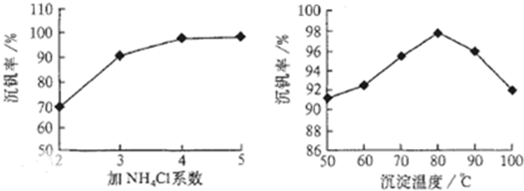
则:反应①②③④中属于氧化还原反应的是______(填数字序号),反应①的离子方程式为______.该工艺中反应③的沉淀率(又称沉矾率)是回收钒的关键之一,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据下图试建议控制氯化铵系数和度:______、______.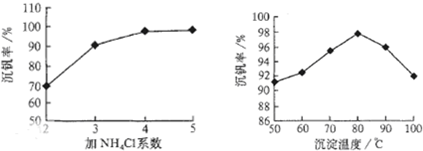
解:(1)以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收;其中二氧化硫的催化氧化在催化剂表面和空气中的氧气接触反应,若气体中含有杂质气体容易使催化剂中毒,所以煅烧黄铁矿形成的炉气必须经除尘、洗涤、干燥;故答案为:接触室,防止催化剂中毒.
(2)依据图1中的转化关系,V2O5参与反应先做氧化剂把二氧化硫氧化为三氧化硫,本身被还原为图中产物V2O4;根据氧化还原反应的实质写出并配平a步化学方程式SO2+V2O5?SO3+V2O4;C是VOSO4转化为SO3,此过程需要重新生成催化剂V2O5,需要氧化剂完成,此过程中的氧化剂时氧气,根据化合价的变化写出C步化学方程式 4VOSO4+O2?2V2O5+4SO3;故答案为:4VOSO4+O2?2V2O5+4SO3
(3)2SO2+O2 2SO3 体系总压强为0.10M Pa,此时二氧化硫的转化率为80%
2SO3 体系总压强为0.10M Pa,此时二氧化硫的转化率为80%
2SO2 +O2 2SO3
2SO3
起始量(mol) 2 1 0
变化量(mol) 2×0.8 0.8 2×0.8
平衡量(mol) 0.4 0.2 1.6
平衡时各物质的浓度为:[SO2]=0.08mol/L,[O2]=0.04mol/L,[SO3]=0.32mol/L,代入平衡常数的计算式得到平衡常数K=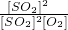 =400 L?mol-1,
=400 L?mol-1,
从图象中可以看出,常压SO2就可以达到较高的转化率,压强的增加引起SO2转化率的变化并不明显,所以工业上直接采用常压;
故答案为:400 L?mol-1,使用常压SO2就可以达到较高的转化率;
(4)依据离子交换法回收钒的新工艺流程图分析反应过程中:
①的目的是把难溶的五氧化二钒还原为溶于水的VOSO4;
②的目的是用KClO3还原为VOSO4为(VO2)2SO4;
③因为NH4VO3难溶于水,此步骤的目的是沉淀VO3-
④是分解NH4VO3得到V2O5;
工艺中反应③的沉淀率(又称沉矾率)是回收钒的关键之一,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据图示分析数据,80℃时沉矾率最高为98%,所以加NH4Cl的系数从图中读出为4;
故答案为:①②;V2O5+SO32-+4H+=2VO2++SO42-+2H2O;4和80℃;
分析:(1)煅烧黄铁矿形成的炉气主要是二氧化硫气体,进入接触室前必须对气体继续除尘、洗涤、干燥,防止催化剂中毒,影响催化氧化的效果;
(2)根据催化剂参与反应过程生成的中间产物,分析催化剂参与反应,最终重新生成来书写化学方程式;
(3)根据化学平衡计算的三段式进行计算,压强的增加引起SO2转化率的变化并不明显,所以工业上直接采用常压;
(4)根据流程中钒元素的存在化合物中的化合价的变化,判断出发生氧化还原反应的是①②;反应①是利用亚硫酸钠在酸性溶液中的还原性把难溶的V2O5转化为易溶于水的VOSO4便于钒的提取;根据图1和图2分析坐标系中的表示含义,结合图②中的沉矾率在80度C时最大,约为98%,在图①中找到对应沉矾率98%下的控制氯化铵系数为4.
点评:本题考查了工业制硫酸的生产步骤、原理应用、注意问题,化学平衡的应用和条件选择,利用信息进行判断和书写化学方程式的能力,图象分析能力,提取钒元素的流程分析和氧化还原反应的应用.
(2)依据图1中的转化关系,V2O5参与反应先做氧化剂把二氧化硫氧化为三氧化硫,本身被还原为图中产物V2O4;根据氧化还原反应的实质写出并配平a步化学方程式SO2+V2O5?SO3+V2O4;C是VOSO4转化为SO3,此过程需要重新生成催化剂V2O5,需要氧化剂完成,此过程中的氧化剂时氧气,根据化合价的变化写出C步化学方程式 4VOSO4+O2?2V2O5+4SO3;故答案为:4VOSO4+O2?2V2O5+4SO3
(3)2SO2+O2
 2SO3 体系总压强为0.10M Pa,此时二氧化硫的转化率为80%
2SO3 体系总压强为0.10M Pa,此时二氧化硫的转化率为80%2SO2 +O2
 2SO3
2SO3 起始量(mol) 2 1 0
变化量(mol) 2×0.8 0.8 2×0.8
平衡量(mol) 0.4 0.2 1.6
平衡时各物质的浓度为:[SO2]=0.08mol/L,[O2]=0.04mol/L,[SO3]=0.32mol/L,代入平衡常数的计算式得到平衡常数K=
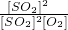 =400 L?mol-1,
=400 L?mol-1,从图象中可以看出,常压SO2就可以达到较高的转化率,压强的增加引起SO2转化率的变化并不明显,所以工业上直接采用常压;
故答案为:400 L?mol-1,使用常压SO2就可以达到较高的转化率;
(4)依据离子交换法回收钒的新工艺流程图分析反应过程中:
①的目的是把难溶的五氧化二钒还原为溶于水的VOSO4;
②的目的是用KClO3还原为VOSO4为(VO2)2SO4;
③因为NH4VO3难溶于水,此步骤的目的是沉淀VO3-
④是分解NH4VO3得到V2O5;
工艺中反应③的沉淀率(又称沉矾率)是回收钒的关键之一,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据图示分析数据,80℃时沉矾率最高为98%,所以加NH4Cl的系数从图中读出为4;
故答案为:①②;V2O5+SO32-+4H+=2VO2++SO42-+2H2O;4和80℃;
分析:(1)煅烧黄铁矿形成的炉气主要是二氧化硫气体,进入接触室前必须对气体继续除尘、洗涤、干燥,防止催化剂中毒,影响催化氧化的效果;
(2)根据催化剂参与反应过程生成的中间产物,分析催化剂参与反应,最终重新生成来书写化学方程式;
(3)根据化学平衡计算的三段式进行计算,压强的增加引起SO2转化率的变化并不明显,所以工业上直接采用常压;
(4)根据流程中钒元素的存在化合物中的化合价的变化,判断出发生氧化还原反应的是①②;反应①是利用亚硫酸钠在酸性溶液中的还原性把难溶的V2O5转化为易溶于水的VOSO4便于钒的提取;根据图1和图2分析坐标系中的表示含义,结合图②中的沉矾率在80度C时最大,约为98%,在图①中找到对应沉矾率98%下的控制氯化铵系数为4.
点评:本题考查了工业制硫酸的生产步骤、原理应用、注意问题,化学平衡的应用和条件选择,利用信息进行判断和书写化学方程式的能力,图象分析能力,提取钒元素的流程分析和氧化还原反应的应用.

练习册系列答案
相关题目

 工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题:
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题: