题目内容
A是单质,D是A单质所含元素的最高价氧化物对应的水化物,甲、乙、丙、丁四种化合物间除甲与丁、丙与乙外,两两均能发生中和反应.已知有如下转化关系(部分产物和反应条件已略去);

试回答:
(1)写出B在工业生产中的一种用途 .
(2)写出B转化为C的可能的离子方程式 .
(3)若C的溶液显酸性,用离子方程式表示其净水的原理 .

试回答:
(1)写出B在工业生产中的一种用途
(2)写出B转化为C的可能的离子方程式
(3)若C的溶液显酸性,用离子方程式表示其净水的原理
考点:无机物的推断
专题:
分析:A是单质,与氧气反应生成B为氧化物,甲、乙、丙、丁四种化合物间除甲与丁、丙与乙外,两两均能发生中和反应,为酸与碱的反应,甲与丁为同类物质,丙与乙为同类物质,氧化物B能与酸或碱反应生成C,D是A单质所含元素的最高价氧化物的水化物,结合转化关系,可推知B为Al2O3,则A为Al、C为Al(OH3),
(1)氧化铝可以制备Al(或作耐火材料)等;
(2)B转化生成C为氧化铝与强碱或强酸的反应;
(3)若C的溶液显酸性,则C为铝盐,溶液中铝离子水解生成氢氧化铝胶体,可以净水;
(1)氧化铝可以制备Al(或作耐火材料)等;
(2)B转化生成C为氧化铝与强碱或强酸的反应;
(3)若C的溶液显酸性,则C为铝盐,溶液中铝离子水解生成氢氧化铝胶体,可以净水;
解答:
解:A是单质,与氧气反应生成B为氧化物,甲、乙、丙、丁四种化合物间除甲与丁、丙与乙外,两两均能发生中和反应,为酸与碱的反应,甲与丁为同类物质,丙与乙为同类物质,氧化物B能与酸或碱反应生成C,D是A单质所含元素的最高价氧化物的水化物,结合转化关系,可推知B为Al2O3,则A为Al、C为Al(OH3),则:
(1)Al2O3在工业上制备Al(或作耐火材料),
故答案为:工业上制备Al(或作耐火材料);
(2)B转化生成C为氧化铝与强碱或强酸的反应,反应离子方程式为:Al2O3+6H+=2Al3++3H2O 或Al2O3+2OH-=AlO2-+H2O,
故答案为:Al2O3+6H+=2Al3++3H2O 或Al2O3+2OH-=AlO2-+H2O;
(3)若C的溶液显酸性,则C为铝盐,溶液中铝离子水解Al3++3H2O?Al(OH)3(胶体)+3H+,生成氢氧化铝胶体,可以净水,
故答案为:Al3++3H2O Al(OH)3(胶体)+3H+.
Al(OH)3(胶体)+3H+.
(1)Al2O3在工业上制备Al(或作耐火材料),
故答案为:工业上制备Al(或作耐火材料);
(2)B转化生成C为氧化铝与强碱或强酸的反应,反应离子方程式为:Al2O3+6H+=2Al3++3H2O 或Al2O3+2OH-=AlO2-+H2O,
故答案为:Al2O3+6H+=2Al3++3H2O 或Al2O3+2OH-=AlO2-+H2O;
(3)若C的溶液显酸性,则C为铝盐,溶液中铝离子水解Al3++3H2O?Al(OH)3(胶体)+3H+,生成氢氧化铝胶体,可以净水,
故答案为:Al3++3H2O
 Al(OH)3(胶体)+3H+.
Al(OH)3(胶体)+3H+.
点评:本题考查无机物推断、盐类水解等,难度中等,B是氧化物且能与酸、碱反应是推断突破口,答题时注意元素化合物知识的灵活运用.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
下列叙述错误的是( )
| A、制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
| B、SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、用AgNO3溶液可以鉴别KCl和KI |
关于原子核外电子运动及描述的说法,不正确的是( )
| A、氢原子核外电子云图,表示氢原子的核外电子的运动轨迹 |
| B、多电子原子核外电子,是按照电子的能量由低到高的顺序,从近到远排列 |
| C、多电子原子核外电子可以根据其能量不同分成K、L、M、N …等不同的能层 |
| D、从第二能层开始,每个能层里面又可以分成几个能级,如s、p、d、f…等 |
在盛放浓硫酸的试剂瓶上应印有如图所示警示标记中的( )
A、 |
B、 |
C、 |
D、 |
只用一种试剂可以区别NH4Cl、MgCl2、FeCl2、AlCl3、FeCl3五种溶液,这种试剂是( )
| A、氨水 | B、NaOH溶液 |
| C、稀硫酸 | D、浓硝酸 |
下列实验误差分析错误的是( )
| A、用湿润的pH试纸测稀碱溶液的pH,测定值偏小 |
| B、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C、滴定前滴定管尖嘴内有气泡,终点读数时尖嘴内无气泡,所测体积偏大 |
| D、测定1mol气体体积时,未冷却至室温就读数,所测体积偏大 |
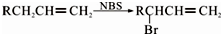 .
.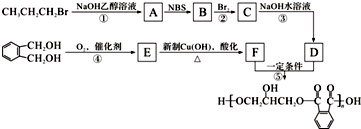
 的同分异构体中同时符合下列条件的芳香族化合物共有
的同分异构体中同时符合下列条件的芳香族化合物共有 某溶液中可能大量含有Mg2+,Cu2+,Al3+,Cl-,OH-,CO32-.当加入氢氧化钠溶液时,生成白色沉淀的物质的量与加入氢氧化钠的物质的量关系如图所示.
某溶液中可能大量含有Mg2+,Cu2+,Al3+,Cl-,OH-,CO32-.当加入氢氧化钠溶液时,生成白色沉淀的物质的量与加入氢氧化钠的物质的量关系如图所示.