题目内容
现由C6H12,CH3CHO,CH3COOH组成的混合物,已知O质量分数为a%,则碳的质量分数为( )
A、
| ||
| B、1-a% | ||
C、
| ||
D、
|
考点:元素质量分数的计算
专题:有机物分子组成通式的应用规律
分析:三种化合物中碳、氢元素的原子个数比都为1:2,故碳元素和氢元素的质量比都为:12:1×2=6:1,混合物中一共有三种元素,氧的质量分数为a%,碳、氢元素的质量分数之和为1-a%,然后结合C、H质量比可计算出碳元素的质量分数.
解答:
解:已知O质量分数为a%,故C和H的质量分数之和为(1-a%);三种化合物中碳、氢元素的原子个数比都为1:2,故碳元素和氢元素的质量比都为:12:1×2=6:1,故碳的质量分数为
×(1-a%)=
(1-a%),
故选D.
| 6 |
| 6+1 |
| 6 |
| 7 |
故选D.
点评:本题考查混合物中元素质量分数的计算,难度中等.根据化学式确定混合物中C、H质量比是解题的关键.

练习册系列答案
相关题目
下列物质中,不能使酸性高锰酸钾溶液褪色的是( )
| A、乙烷 | B、乙烯 |
| C、乙炔 | D、二氧化硫 |
用价层电子对互斥理论预测H2O和CH4的立体结构两个结论都正确的是( )
| A、直线形,三角锥形 |
| B、V形,三角锥形 |
| C、直线形,正四面体形 |
| D、V形,正四面体形 |
下列氧化物不属于酸性氧化物的是( )
| A、SiO2 |
| B、Mn2O7 |
| C、CO |
| D、N2O5 |
下列化合物中,常温下能被空气氧化的是( )
A、 |
B、 |
C、 |
| D、CH4 |
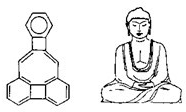 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛(如图).因而称为释迦牟尼分子(所有原子在同一平面).有关该有机分子的说法不正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛(如图).因而称为释迦牟尼分子(所有原子在同一平面).有关该有机分子的说法不正确的是( )| A、该有机物属于芳香烃 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子中含有22个碳原子 |
| D、该有机物可发生加成反应 |
实验室制取少量N2的反应是NaNO2+NH4Cl═NaCl+N2↑+2H2O,下列说法正确的是( )
| A、NaNO2是氧化剂 |
| B、NH4Cl发生还原反应 |
| C、生成1mol的 N2转移3mol的电子 |
| D、NaNO2在反应中失电子 |
下列溶液一定呈中性的是( )
| A、将pH=5的盐酸稀释100倍所得溶液 |
| B、c(H+)=1.0×10-7mol/L |
| C、c(H+)=c(OH-)=1×10-6mol/L的溶液 |
| D、非电解质溶于水得到的溶液 |